
科目:高中化學 來源:2016-2017學年云南省高二上期中化學卷(解析版) 題型:填空題
2016年9月15日“天宮二號空間實驗室發射任務圓滿成功”中國載人航天工程進入嶄新時期。其 中火箭推進器中盛有強還原劑液態肼(N2H4)和強氧化劑液態雙氧水。當它們混合反應時,即產生大量氮氣和水蒸氣,并放出大量的熱。已知0.2mol液態肼與足量的液態雙氧水反應,生成氮氣和水蒸氣,放出128.3kJ的熱量。
中火箭推進器中盛有強還原劑液態肼(N2H4)和強氧化劑液態雙氧水。當它們混合反應時,即產生大量氮氣和水蒸氣,并放出大量的熱。已知0.2mol液態肼與足量的液態雙氧水反應,生成氮氣和水蒸氣,放出128.3kJ的熱量。
(1)已知H2O(l)=H2O(g) ΔH=+44kJ·mol-1。則8g液態肼與液態雙氧水反應生成液態水時放出的熱量是___________kJ。
(2)已知:N2(g)+2O2(g)=2NO2(g) ΔH=+67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-534kJ·mol-1
氣態肼和二氧化氮反應的熱化學方程式為 。
(3)火箭和導彈表面的薄層是耐高溫物質。將石墨、鋁粉、二氧化鈦按一定比例混合在高溫下煅燒,所得物質可作耐高溫材料,4Al(s)+3TiO2(s)+3C(s)=2 Al2O3(s)+3TiC(s) ΔH=-1176kJ·mol-1,則反應過程中,每轉移0.3mol電子放出的熱量為 kJ。
Al2O3(s)+3TiC(s) ΔH=-1176kJ·mol-1,則反應過程中,每轉移0.3mol電子放出的熱量為 kJ。
查看答案和解析>>
科目:高中化學 來源:2017屆內蒙古高三上月考四化學卷(解析版) 題型:實驗題
海水是寶貴的資源寶庫,目前氯堿工業、海水提鎂、海水提溴為人類提供了大量工業原料。下圖是海水綜合利用的部分流程圖,據圖回答問題:

(1)由海水曬制的粗鹽中含有Ca2+、Mg2+、SO42-等離子,為除去這些離子,所加試劑及其先后順序為(寫化學式) _____________________。
(2)①目前 較先進的電解制堿法是離子交換膜電解法,即用陽離子交換膜把電解槽隔成陰極室和陽極室,其作用是______________,電解飽和食鹽水的化學反應方程式為_____________。
較先進的電解制堿法是離子交換膜電解法,即用陽離子交換膜把電解槽隔成陰極室和陽極室,其作用是______________,電解飽和食鹽水的化學反應方程式為_____________。
②制取MgCl2的過程中涉及反應:MgCl2·6H2O MgCl2+6H2O,該反應要在HCl氣氛中進行,其原因是_____________________。
MgCl2+6H2O,該反應要在HCl氣氛中進行,其原因是_____________________。
(3)苦鹵中先通入Cl2置換出Br2 ,為什么吹出后用SO2吸收轉化為Br-再用Cl2置換,其理由是_________,由此判斷Cl2、Br2、SO2的氧化性由強到弱的順序為_______________。
(4)也有工藝是在吹出Br2后用碳酸鈉溶液吸收,形成溴化鈉和溴酸鈉,同時有CO2放出。該反應的離子方程式是_____________;最后再用H2SO4處理得到Br2 ,之后加入CCl4進行Br2的萃取,最終用_____________方法得到單質Br2。
查看答案和解析>>
科目:高中化學 來源:2017屆遼寧省高三上模擬一化學試卷(解析版) 題型:選擇題
某恒定溫度下,在一個2 L的密閉容器中充入A氣體、B氣體,測得其濃度2 mol/L和1 mol/L;且發生如下反應:3A(g)+2B(g)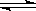 2C(?)+3D(?)ΔH =+a kJ·mol-1,已知“?”代表C、D狀態未確定;反應一段時間后達到平衡,測得生成1.6 mol C,且反應前后壓強比為5∶3,則下列說法中正確的是
2C(?)+3D(?)ΔH =+a kJ·mol-1,已知“?”代表C、D狀態未確定;反應一段時間后達到平衡,測得生成1.6 mol C,且反應前后壓強比為5∶3,則下列說法中正確的是
A.保持體積不變的情況下,向該體系中充入He氣,反應速率加快,平衡正動
B.此時B的轉化率為20%
C.增大該體系壓強,平衡向右移動,但化學平衡常數不變
D.增加C的量,A、B轉化率減小,ΔH減小
查看答案和解析>>
科目:高中化學 來源:2017屆遼寧省高三上模擬一化學試卷(解析版) 題型:選擇題
下列說法正確的是
A.一定條件下,使用催化劑能加快反應速率并提高反應物的平衡轉化率
B.氨水加水稀釋后,溶液中c(NH3·H2O)/c(NH )的值增大
)的值增大
C.需要加熱才能發生的反應不一定是吸熱反應
D.電解精煉銅時,陰極溶解銅的質量小于陽極析出銅的質量
查看答案和解析>>
科目:高中化學 來源:2017屆江西師大附中高三上學期期中化學試卷(解析版) 題型:實驗題
硫代硫酸鈉是一種重要的化工產品。某興趣小組擬制備硫代硫酸鈉晶體(Na2S2O3·5H2O)。
Ⅰ.[查閱資料]
(1)Na2S2O3·5H2O是無色透明晶體,易溶于水,其稀溶液與BaCl2溶液混合無沉淀生成。
(2)向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3,所得產品常含有少量Na2SO3和Na2SO4。
Ⅱ.[制備產品]實驗裝置如圖所示(省略夾持裝置):
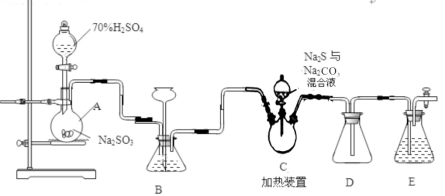
燒瓶C中發生反應如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq)(I)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l)(II)
S(s)+Na2SO3(aq) Na2S2O3(aq)(III)
Na2S2O3(aq)(III)
實驗步驟:
①待Na2S和Na2CO3完全消耗后,結束反應。
②向C中燒瓶加入Na2S和Na2CO3混合溶液
③檢查裝置氣密性,按圖示加入試劑。
④向A中燒瓶滴加濃H2SO4。
⑤過濾C中混合物,濾液經蒸發、結晶、過濾、洗滌、干燥,得到產品。
(1)E中的試劑是____________(選填下列字母編號)。
A.稀H2SO4 B.NaOH溶液 C.飽和NaHSO3溶液
(2)正確的操作順序是
(3)裝置B的作用之一是觀察SO2的生成速率,其中的液體最好選擇 。
a.蒸餾水 b.飽和Na2SO3溶液
c.飽和NaHSO3溶液 d.飽和NaHCO3溶液
Ⅲ.[探究與反思]
(1)為驗證產品中含有Na2SO3和Na2SO4,該小組設計了以下實驗方案,請將方案補充完整。(所需試劑從稀HNO3、稀H2SO4、稀HCl、蒸餾水中選擇)
取適量產品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,________________ ,若沉淀未完全溶解,并有刺激性氣味的氣體產生,則可確定產品中含有Na2SO3和Na2SO4。
(2)為減少裝置C中生成Na2SO4的量,在不改變原有裝置的基礎上對實驗步驟(2)進行了改進,改進后的操作是___________________。
(3)Na2S2O3·5H2O的溶解度隨溫度升高顯著增大,所得產品通過____________方法提純。
查看答案和解析>>
科目:高中化學 來源:2017屆江西師大附中高三上學期期中化學試卷(解析版) 題型:選擇題
氯氣溶于水達到平衡后,若其他條件不變,只改變某一條件,下列敘述正確的是( )
A.加入少量水,水的電離平衡向正反應方向移動
B.通入少量SO2,溶液漂白性增強
C.加入少量固體NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
D.再通入少量氯氣, 減小
減小
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省高三上學期期中化學卷(解析版) 題型:選擇題
一定條件下進行反應:COCl2(g) Cl2(g)+CO(g)。向2.0 L恒容密閉容器中充入1.0 mol COCl2(g),經過一段時間后達到平衡。反應過程中測得的有關數據見下表:
Cl2(g)+CO(g)。向2.0 L恒容密閉容器中充入1.0 mol COCl2(g),經過一段時間后達到平衡。反應過程中測得的有關數據見下表:
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
下列說法正確的是( )
A.保持其他條件不變,升高溫度,平衡時c(Cl2)=0.22 mol·L-1,則反應的ΔH<0
B.若在2 L恒容絕熱(與外界沒有熱量交換)密閉容器進行該反應,化學平衡常數不變
C.保持其他條件不變,起始向容器中充入1.2 mol COCl2、0.60 mol Cl2和0.60 mol CO,反應達到平衡前的速率:v(正)>v(逆)
mol COCl2、0.60 mol Cl2和0.60 mol CO,反應達到平衡前的速率:v(正)>v(逆)
D.保持其他條件不變,起始向容器中充入1.0 mol Cl2和0.8 mol CO,達到平衡時,Cl2的轉化率小于60%
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江省哈爾濱市四校高一期中聯考化學試卷(解析版) 題型:填空題
分析下列反應回答相應問題。
(1)3Cu+8HNO3=3Cu(NO3)2+ 2NO↑+4H2O未被還原的硝酸與參加反應的總硝酸的質量比為 。
2NO↑+4H2O未被還原的硝酸與參加反應的總硝酸的質量比為 。
(2)S+2KNO3+3C K2S+N2↑+3CO2↑ 還原劑是 還原產物是
K2S+N2↑+3CO2↑ 還原劑是 還原產物是
(3)3Cl2+6NaOH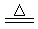 5NaCl+NaClO3+3H2O 反應中若消耗3molCl2共轉移 mol電子
5NaCl+NaClO3+3H2O 反應中若消耗3molCl2共轉移 mol電子
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com