
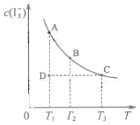
 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物質的量濃度c(I3-)與溫度T的關系如圖所示(曲線上任何一點都表示平衡狀態,忽略I2 的揮發).下列說法正確的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物質的量濃度c(I3-)與溫度T的關系如圖所示(曲線上任何一點都表示平衡狀態,忽略I2 的揮發).下列說法正確的是( )| A. | 反應 I2(aq)+I-(aq)?I3-(aq)△H>0 | |
| B. | 狀態A與狀態B相比,狀態A的c(I2)大 | |
| C. | 若反應進行到狀態D時,一定有v逆>v正 | |
| D. | 若溫度為T1、T2,反應的平衡常數K1、K2則 K1>K2 |
分析 由圖象曲線的變化趨勢可知,當溫度升高時,I3-的物質的量濃度減小,說明平衡向逆反應方向移動,該反應的正反應為放熱反應;升高溫度,平衡向逆反應方向移動,溫度越高,平衡常數越小,從溫度對平衡移動的影響分別判斷碘單質的轉化率、平衡常數的變化、反應進行方向及不同狀態的A的濃度大小,以此解答.
解答 解:A.由圖象曲線的變化趨勢可知,當溫度升高時,I3-的物質的量濃度減小,說明該反應的正反應為放熱反應,反應I2(aq)+I-(aq)?I3-(aq)的△H<0,故A錯誤;
B.溫度升高,平衡向逆方向移動,c(I3-)變小,則c(I2)應變大,所以狀態B的c(I2)大,故B錯誤;
C.若反應進行到狀態D時,反應未達到平衡狀態,若反應趨向于平衡,則反應向生成的I3-方向移動,則v正>v逆,故C錯誤;
D.該反應的正反應為放熱反應,升高溫度,平衡向逆反應方向移動,溫度越高,平衡常數越小,若溫度為T1、T2,反應的平衡常數分別為K1、K2,則K1>K2,故D正確.
故選D.
點評 本題考查化學平衡移動圖象問題,為高頻考點,題目難度中等,注意根據圖象曲線變化分析化學方程式的特征以及溫度、濃度、壓強對平衡移動的影響,試題培養了學生的分析、理解能力及靈活應用所學知識的能力.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:2016-2017學年甘肅省高二上10月月考化學試卷(解析版) 題型:填空題
下列化合物:①HCl ②NaOH ③CH3COOH ④NH3·H2O ⑤CH3COONa ⑥NH4Cl
(1)溶液呈堿性的有____________(填序號)。
(2)常溫下0.01 mol/L HCl溶液的pH=____________;0.01 mol/L NaOH溶液的pH=______________;pH=11的CH3COONa溶液中由水電離產生的c(OH-) =___________。
HCl溶液的pH=____________;0.01 mol/L NaOH溶液的pH=______________;pH=11的CH3COONa溶液中由水電離產生的c(OH-) =___________。
(3)將等PH等體積的HCl和CH3COOH分別稀釋m倍和n倍,稀釋后兩溶液的PH仍相等,則m___________n (填“大于、等于、小于”)。
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 水電離產生的c(H+):①=③>④=② | |
| B. | 將②、③溶液混合后,pH=7,消耗溶液的體積:②>③ | |
| C. | 等體積的①、②、④溶液分別與足量鋁粉反應,生成H2的量;②最大 | |
| D. | 向溶液中加入100mL水后,溶液的pH:③>④>①>② |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 高錳酸鉀是氧化劑,Na2O2既是氧化劑,又是還原劑 | |
| B. | 反應的氧化產物Mn2+ | |
| C. | 當反應產生標準狀況下2.24L O2 時,反應轉移的電子為0.2mol | |
| D. | 向高錳酸鉀溶液滴加濃鹽酸可以得到酸性高錳酸鉀溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com