
【題目】化合物H是一種光伏材料中間體。工作室由芳香化合物A制備H的一種合成路線如下:
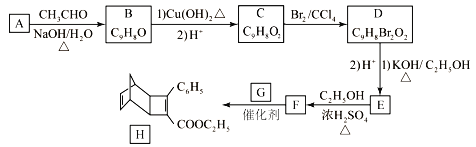
已知:①RCHO+CH3CHO ![]() RCH=CHCHO+H2O
RCH=CHCHO+H2O
②![]()
回答下列問題
(1)B所含官能團名稱為___________。
(2)由B生成C和E生成F的反應類型分別為___________、___________。
(3)D的結構簡式為___________。
(4)由A生成B的化學方程式為___________。
(5)芳香化合物X是F的同分異構體,X能與飽和碳酸氫鈉溶液反應放出CO2,其核磁共振氫譜顯示有4種不同化學環境的氫,峰面積比為6:2:1:1,符合要求的X的結構有___________種,寫出其中一種結構簡式___________。
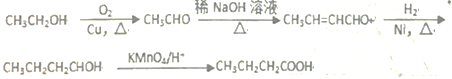
(6)根據已有知識并結合相關信息,寫出以乙醇為原料合成 CH3CH2CH2COOH的合成路線(無機試劑在用)(合成路線示例如下:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH ______________________________________________。
CH3CH2OH ______________________________________________。
【答案】碳碳雙鍵、醛基 氧化反應 取代反應(或酯化反應) ![]()
![]() 4種
4種 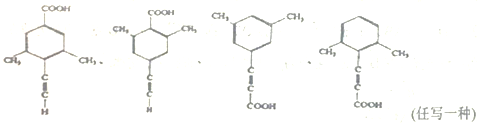
【解析】
芳香族化合物A與乙醛發生信息①中的反應生成B,A含有醛基,反應中脫去1分子水,由原子守恒可知A的分子式為:C9H8O+H2O-C2H4O=C7H6O,故A為![]() ,則B為
,則B為![]() ,B發生氧化反應、酸化得到C為
,B發生氧化反應、酸化得到C為![]() .C與溴發生加成反應得到D為
.C與溴發生加成反應得到D為![]() ,D發生消去反應、酸化得到E為
,D發生消去反應、酸化得到E為![]() .E與乙醇發生酯化反應生成F為
.E與乙醇發生酯化反應生成F為![]() .結合信息②中的加成反應、H的結構簡式,可推知G為
.結合信息②中的加成反應、H的結構簡式,可推知G為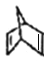 ,以此解答(1)~(5);
,以此解答(1)~(5);
(6)利用信息①增長碳鏈,乙醇催化氧化生成乙醛,2分子乙醛反應得到CH3CH=CHCHO,再與氫氣發生反應得到CH3CH2CH2CH2OH,最后用酸性高錳酸鉀溶液氧化得到CH3CH2CH2COOH。
(1)由分析可知,B為![]() ,所含官能團名稱為碳碳雙鍵和醛基。
,所含官能團名稱為碳碳雙鍵和醛基。
(2)![]() 發生氧化反應生成的C為
發生氧化反應生成的C為![]() ;E為
;E為![]() ,其與乙醇發生酯化反應生成的F為
,其與乙醇發生酯化反應生成的F為![]() ,反應類型為取代反應;
,反應類型為取代反應;
(3)由分析可知D的結構簡式為![]() ;
;
(4)A為![]() ,與乙醛在NaOH的水溶液中發生反應生成的B為
,與乙醛在NaOH的水溶液中發生反應生成的B為![]() ,反應的化學方程式為
,反應的化學方程式為![]() ;
;
(5)F為![]() ,芳香化合物X是F的同分異構體,X能與飽和碳酸氫鈉溶液反應放出CO2,說明含有羧基,其核磁共振氫譜顯示有4種不同化學環境的氫,峰面積比為6:2:1
,芳香化合物X是F的同分異構體,X能與飽和碳酸氫鈉溶液反應放出CO2,說明含有羧基,其核磁共振氫譜顯示有4種不同化學環境的氫,峰面積比為6:2:1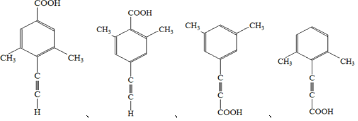 ;
;
(6)利用信息①增長碳鏈,乙醇催化氧化生成乙醛,2分子乙醛反應得到CH3CH=CHCHO,再與氫氣發生反應得到CH3CH2CH2CH2OH,最后用酸性高錳酸鉀溶液氧化得到CH3CH2CH2COOH.合成路線流程圖為: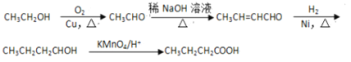 。
。


科目:高中化學 來源: 題型:
【題目】能源是國民經濟發展的重要基礎,我國目前使用的能源主要是化石燃料。
(1)在25 ℃、101 kPa時,16 g CH4完全燃燒生成液態水時放出的熱量是890.31 kJ,則CH4燃燒的熱化學方程式是 。
(2)已知:C(s)+ O2(g)![]() CO2(g) ΔH=-437.3 kJmol-1
CO2(g) ΔH=-437.3 kJmol-1
H2(g)+ ![]() O2(g)
O2(g)![]() H2O(g) ΔH=-285.8 kJmol-1
H2O(g) ΔH=-285.8 kJmol-1
CO(g)+ ![]() O2(g)
O2(g)![]() CO2(g) ΔH=-283.0 kJmol-1
CO2(g) ΔH=-283.0 kJmol-1
則煤的氣化主要反應的熱化學方程式是
C(s)+ H2O(g)![]() CO(g)+ H2(g) ΔH= kJmol-1。
CO(g)+ H2(g) ΔH= kJmol-1。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】阿司匹林(結構如圖)是一種歷史悠久的解熱鎮痛藥,誕生于1899年3月6日。用于治感冒、發熱、頭痛、牙痛、關節痛、風濕病,還能抑制血小板聚集,用于預防和治療缺血性心臟病、心絞痛、心肺梗塞、腦血栓形成,應用于血管形成術及旁路移植術也有效。

(1)阿司匹林水溶液呈_____(填“酸性”、“堿性”、“中性”)。
(2)阿司匹林分子中虛線框內官能團的名稱______(填名稱)。
(3)阿司匹林必須密閉干燥存儲,以防止在酸性條件下與水發生_______ 生成乙酸和水楊酸( ![]() )
)
A.水解反應 B.加成反應 C.酯化反應
(4)向阿司匹林水溶液中滴加飽和NaHCO3溶液,實驗現象為______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上,以鈦鐵礦(主要含FeTiO3,還含有Fe2O3 和Al2O3、SiO2等雜質)為原料制備二氧化鈦并得到副產品綠礬(FeSO4·7H2O)的工藝流程如下圖所示。
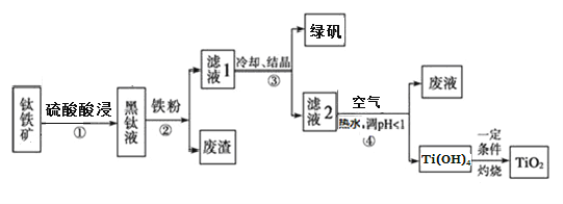
已知:TiO2+在一定條件下會發生水解。
回答下列問題:
(1)要提高酸浸時鈦礦石的溶解速率,可行的措施是(寫一條即可)_______________。黑鈦液中生成的主要陽離子有TiO2+和Fe2+,步驟①主要反應的化學方程式是_________。
(2)步驟②中,加入鐵粉的主要作用是_____,同時也會將部分TiO2+還原為Ti3+。
(3)向濾液2中通入空氣的目的是______(用離子方程式表示)。
(4)請結合化學用語用化學平衡理論解釋步驟④中加入熱水稀釋將TiO2+轉化為Ti(OH)4 的原因:_________________。
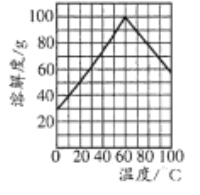
(5)副產品綠礬中含有雜質[Al2(SO4)3]。要將副產品進一步提純,請結合右圖的綠礬溶解度曲線完成提純過程:將副產品溶于稀硫酸中,充分攪拌后,用NaOH溶液調節反應液的pH約為5,過濾沉淀后得到FeSO4溶液,______,過濾,用冰水洗滌,低溫干燥,得到FeSO4·7H20晶體。
(6)用氧化還原滴定法測定制備得到的產品中TiO2的質量分數:在一定條件下,將一定量的產品溶解并將TiO2還原為Ti3+,再以KSCN溶液作為指示劑,用硫酸鐵銨[NH4Fe(SO4)2]標準溶液滴定Ti3+至全部生成Ti4+。
①滴定終點的現象是_______________。
②滴定分析時,稱取TiO2試樣0.2 g,消耗0.1 mol/L NH4Fe(SO4)2標準溶液24.00mL,則TiO2的質量分數為_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,下列說法正確的是( )
A.將pH=2的酸溶液稀釋10倍,溶液的pH一定變為3
B.將pH=2的鹽酸溶液和pH=4的鹽酸溶液等體積混合后,溶滾的pH變為3
C.將pH=12的Ba(OH)2溶液稀釋10倍,溶液的pH變為13
D.將pH=a的鹽酸與pH=b的NaOH溶液等體積混合后,若pH=7, 則a+b=14
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學生用0.100 mol·L-1的KOH標準溶液滴定未知濃度的鹽酸,其操作可分解為如下幾步:
A.移取20 mL待測鹽酸溶液注入潔凈的錐形瓶中,并加入2~3滴酚酞;
B.用標準溶液潤洗滴定管2~3次;
C.把盛有標準溶液的堿式滴定管固定好,調節滴定管使尖嘴處充滿溶液;
D.取標準KOH溶液注入堿式滴定管至刻度“0”以上2~3 cm 處;
E.調節液面至“0”或“0”以下刻度,記下讀數;
F.把錐形瓶放在滴定管的下面,用標準KOH溶液滴定至終點并記下滴定管液面的刻度。
就此實驗完成填空:
(1)正確操作步驟的順序是(用序號字母填寫)__________________________。
(2)上述B步驟操作的目的是__________________________________________。
(3)上述A步驟操作之前,若先用待測溶液潤洗錐形瓶,則滴定結果______(填“偏高“、“偏低”或“不變”)
(4)判斷到達滴定終點的實驗現象是________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國科學家研發了一種室溫下“可呼吸”的Na—CO2二次電池。將NaClO4溶于有機溶劑作為電解液,鈉和負載碳納米管的鎳網分別作為電極材料,電池的總反應為:3CO2+4Na![]() 2Na2CO3+C。下列說法錯誤的是
2Na2CO3+C。下列說法錯誤的是

A. 放電時,ClO4-向負極移動
B. 充電時釋放CO2,放電時吸收CO2
C. 放電時,正極反應為:3CO2+4e =2CO32-+C
D. 充電時,正極反應為:Na++e=Na
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】目前,對CO、NOx的綜合利用是科學家研究的熱點。回答下列問題:
(1)已知:N2(g)+O2(g)=2NO(g) H1=+180.5kJ·mol-1
2CO(g)+O2(g)=2CO2(g) H2=-566kJ·mol-1
2NO(g)+O2(g)=2NO2(g) H3=-116.2kJ·mol-1
寫出CO和NO2反應生成N2的熱化學方程式:____。
(2)制備AlCl3的實際生產過程中,常加入足量的碳粉,反應后生成CO(g)。T℃時,向恒容密閉容器中加入3mol Al2O3(s)、8mol C(s)和3.3mol Cl2(g),發生反應。Cl2的濃度變化如圖1所示;圖2為20min后改變容器中條件,平衡體系的反應速率(v)隨時間(t)的變化關系,且四個階段都各改變一種不同的條件。
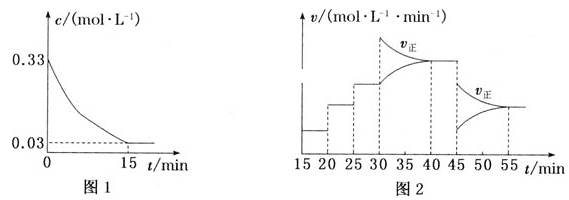
①容器中發生反應的化學方程式為___。
②0~15min內,該反應的平均速率v(CO)=___mol·L-1·min-1。
③T℃時,該反應的平衡常數K=___。
④15min時的平衡常數K(15)、44 min時的平衡常數K(44)與55min時的平衡常數K(55)的大小關系為____。
(3)N2O5在一定條件下可發生分解:2N2O5(g)![]() 4NO2(g)+O2(g)。一定溫度下,在恒容密閉容器中充入一定量N2O5進行該反應,能判斷反應已達到化學平衡狀態的是___(填標號)。
4NO2(g)+O2(g)。一定溫度下,在恒容密閉容器中充入一定量N2O5進行該反應,能判斷反應已達到化學平衡狀態的是___(填標號)。
A.容器中氣體的密度不發生變化
B.NO2和O2的體積比保持不變
C.v正(NO2)=2v逆(N2O5)
D.氣體的平均相對分子質量為43.2,且保持不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硼酸(H3BO3)是一種重要的化工原料,廣泛應用于玻璃、醫藥、肥料等工藝。一種以硼鎂礦(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)為原料生產硼酸及輕質氧化鎂的工藝流程如下:

回答下列問題:
(1)在95 ℃“溶侵”硼鎂礦粉,產生的氣體在“吸收”中反應的化學方程式為_________。
(2)“濾渣1”的主要成分有_________。為檢驗“過濾1”后的濾液中是否含有Fe3+離子,可選用的化學試劑是_________。
(3)根據H3BO3的解離反應:H3BO3+H2O![]() H++B(OH)4,Ka=5.81×1010,可判斷H3BO3是_______酸;在“過濾2”前,將溶液pH調節至3.5,目的是_______________。
H++B(OH)4,Ka=5.81×1010,可判斷H3BO3是_______酸;在“過濾2”前,將溶液pH調節至3.5,目的是_______________。
(4)在“沉鎂”中生成Mg(OH)2·MgCO3沉淀的離子方程式為__________,母液經加熱后可返回___________工序循環使用。由堿式碳酸鎂制備輕質氧化鎂的方法是_________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com