

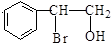 ,F分子中含有的含氧官能團名稱是羥基、羧基(順序可以顛倒).
,F分子中含有的含氧官能團名稱是羥基、羧基(順序可以顛倒). .
. .
.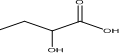 的合成線路:H2C=CHCH2CH3$\stackrel{HBrO}{→}$HOCH2CHBrCH2CH3→CH3CH2CHBrCOOH$\stackrel{NaOH(aq)△}{→}$CH3CH2CHOHCOOH.
的合成線路:H2C=CHCH2CH3$\stackrel{HBrO}{→}$HOCH2CHBrCH2CH3→CH3CH2CHBrCOOH$\stackrel{NaOH(aq)△}{→}$CH3CH2CHOHCOOH. 分析 根據B的分子式知,生成B的反應為加成反應,B中核磁共振氫譜圖顯示分子中有6種不同環境的氫原子,則B結構簡式為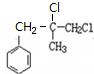 ,B發生水解反應生成C為
,B發生水解反應生成C為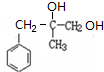 ,C發生氧化反應生成D,結合D分子式知,D為
,C發生氧化反應生成D,結合D分子式知,D為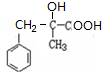 ;
;
苯乙烯與HBrO發生加成反應生成E,E可以氧化反應,根據E氧化產物結構簡式知,E為 ,
,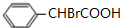 和氫氧化鈉的水溶液反應然后酸化得到F,且D和F是同系物,故F為
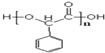
和氫氧化鈉的水溶液反應然后酸化得到F,且D和F是同系物,故F為 ,D與F生成G,G結構中含有三個六元環,則G為
,D與F生成G,G結構中含有三個六元環,則G為 ;
;
(6)H2C=CHCH2CH3和HBrO發生加成反應生成HOCH2CHBrCH2CH3,HOCH2CHBrCH2CH3發生氧化反應生成CH3CH2CHBrCOOH,CH3CH2CHBrCOOH和NaOH水溶液加熱發生取代反應生成CH3CH2CHOHCOOH.
解答 解:根據B的分子式知,生成B的反應為加成反應,B中核磁共振氫譜圖顯示分子中有6種不同環境的氫原子,則B結構簡式為 ,B發生水解反應生成C為
,B發生水解反應生成C為 ,C發生氧化反應生成D,結合D分子式知,D為
,C發生氧化反應生成D,結合D分子式知,D為 ;
;
苯乙烯與HBrO發生加成反應生成E,E可以氧化反應,根據E氧化產物結構簡式知,E為 ,
,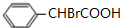 和氫氧化鈉的水溶液反應然后酸化得到F,且D和F是同系物,故F為
和氫氧化鈉的水溶液反應然后酸化得到F,且D和F是同系物,故F為 ,D與F生成G,G結構中含有三個六元環,則G為
,D與F生成G,G結構中含有三個六元環,則G為 ;
;
(1)(CH3)2C═CH2的系統命名法名稱2-甲基-1-丙烯(或2-甲基丙烯,或甲基丙烯),生成B這一步的反應類型為加成反應,
故答案為:2-甲基-1-丙烯(或2-甲基丙烯,或甲基丙烯);加成反應;
(2)E的結構簡式為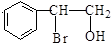 ,F分子中含有的含氧官能團名稱是羥基、羧基(順序可以顛倒),
,F分子中含有的含氧官能團名稱是羥基、羧基(順序可以顛倒),
故答案為: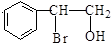 ; 羥基、羧基(順序可以顛倒);
; 羥基、羧基(順序可以顛倒);
(3)C經氧化后可得到一種能與新制銀氨溶液發生銀鏡反應的物質,該物質中含有醛基,該反應方程式為 ,
,
故答案為: ;
;
(4)F可在一定條件下合成高分子化合物,該高分子化合物的結構簡式 ,
,
故答案為: ;
;
(5)D為 ,D的同分異構體符合下列條件:①與FeCl3溶液發生顯色反應,說明含有酚羥基;
,D的同分異構體符合下列條件:①與FeCl3溶液發生顯色反應,說明含有酚羥基;
②苯環上有兩個取代基;
③能與碳酸氫鈉溶液反應放出氣體,說明含有-COOH,
如果取代基為酚-OH、-CH2CH2CH2COOH,有鄰間對三種結構;
如果取代基為酚-OH、-CH(CH3)CH2COOH,有鄰間對三種結構;
如果取代基為酚-OH、-CH2CH(CH3)COOH,有鄰間對三種結構;
如果取代基為酚-OH、-C(CH3)2COOH,有鄰間對三種結構;
如果取代基為酚-OH、-CH(CH2CH3)COOH,有鄰間對三種結構,
所以符合條件的有15種;
故答案為:15;
(6)H2C=CHCH2CH3和HBrO發生加成反應生成HOCH2CHBrCH2CH3,HOCH2CHBrCH2CH3發生氧化反應生成CH3CH2CHBrCOOH,CH3CH2CHBrCOOH和NaOH水溶液加熱發生取代反應生成CH3CH2CHOHCOOH,所以其合成路線為H2C=CHCH2CH3$\stackrel{HBrO}{→}$HOCH2CHBrCH2CH3→CH3CH2CHBrCOOH$\stackrel{NaOH(aq)△}{→}$CH3CH2CHOHCOOH,
故答案為:H2C=CHCH2CH3$\stackrel{HBrO}{→}$HOCH2CHBrCH2CH3→CH3CH2CHBrCOOH$\stackrel{NaOH(aq)△}{→}$CH3CH2CHOHCOOH.
點評 本題考查有機物合成和推斷,為高頻考點,側重考查學生分析推斷及知識綜合運用、知識遷移能力,明確物質之間轉化、物質官能團及其性質關系、反應類型及反應條件是解本題關鍵,難點是合成路線設計及同分異構體種類判斷,題目難度中等.


 千里馬走向假期期末仿真試卷寒假系列答案
千里馬走向假期期末仿真試卷寒假系列答案科目:高中化學 來源: 題型:解答題
 蘊藏在海底的“可燃冰”是高壓下形成的外觀像冰的甲烷水合物固體.根據你所學的知識回答下列問題:
蘊藏在海底的“可燃冰”是高壓下形成的外觀像冰的甲烷水合物固體.根據你所學的知識回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
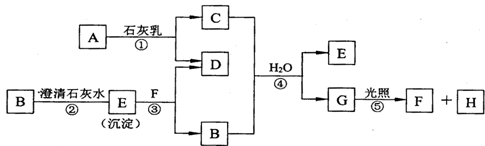
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 氮化鋁(AlN)是一種人工合成的非氧化物陶瓷材料,可在溫度高于1500℃時,通過碳熱還原法制得.實驗研究認為,該碳熱還原反應分兩步進行:①Al2O3在碳的還原作用下生成鋁的氣態低價氧化物X(X中Al與O的質量比為6.75:2);②在碳存在下,X與N2反應生成AlN.請回答:
氮化鋁(AlN)是一種人工合成的非氧化物陶瓷材料,可在溫度高于1500℃時,通過碳熱還原法制得.實驗研究認為,該碳熱還原反應分兩步進行:①Al2O3在碳的還原作用下生成鋁的氣態低價氧化物X(X中Al與O的質量比為6.75:2);②在碳存在下,X與N2反應生成AlN.請回答:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 物質可分為純凈物和混合物 | |
| B. | 碳酸鈉既是鈉鹽也是碳酸鹽 | |
| C. | 氧化物分為金屬氧化物和非金屬氧化物 | |
| D. | 化合物分為電解質和非電解質 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
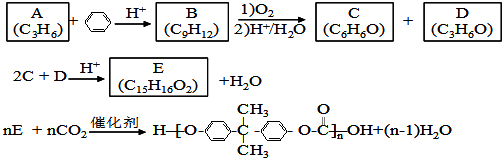
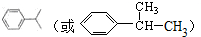 ;
;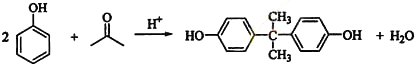 ;
;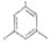 (寫出結構簡式).
(寫出結構簡式).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | N2O 與 CO2均不含非極性鍵 | |
| B. | N2O 的電子式可 | |
| C. | N2O 為三角形分子 | |
| D. | N2O 與 SiO2互為等電子體,具有相似的結構和相似性質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 如圖是M、N兩種不含結晶水的固體物質溶解度曲線.下列說法中正確的是( )
如圖是M、N兩種不含結晶水的固體物質溶解度曲線.下列說法中正確的是( )| A. | t1℃時,N比M的溶解度大 | |
| B. | 溫度從t1℃升高到t3℃時,N的飽和溶液張溶質的質量分數將增大 | |
| C. | M比N的溶解度大 | |
| D. | N中含有少量M時,可用降溫結晶法提純N |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com