
| A. | 放電時,電解質溶液中K+移向負極 | |
| B. | 放電時,電解質溶液的pH 不變 | |
| C. | 充電時,陰極的反應為:Zn(OH)42-+2e-=Zn+4OH- | |
| D. | 充電時,當有4.48L 氧氣(標準狀況下)釋放出來時,則析出固體Zn為13g |
分析 根據2Zn+O2+4OH-+2H2O═2Zn(OH)42-可知,O2中元素的化合價降低,被還原,應為原電池正極,電極反應為:O2+4e-+2H2O=4OH-,Zn元素化合價升高,被氧化,應為原電池負極,電極反應為:Zn-2e-+4OH-=Zn(OH)42-,放電時陽離子向正極移動,充電與放電過程相反,以此解答該題.
解答 解:A.放電時,為原電池,溶液中陽離子向正極移動,即K+向正極移動,故A錯誤;
B.放電時,消耗氫氧根,堿性減弱,PH值減小,故B錯誤;
C.充電時,陽極上發生失電子的氧化反應,陰極上發生得電子的氧化反應,則陰極反應為:Zn(OH)42-+2e-=Zn+4OH-,故C正確;
D.產生1mol氧氣,轉移電子為4mol,充電時,當有4.48L 氧氣(標準狀況下)釋放出來時,轉移電子物質的量為:$\frac{4.48L}{22.4L/mol}$×4=0.8mol,根據Zn~2e-,則析出固體Zn為:$\frac{0.8mol}{2}$×65g/mol=26g,故D錯誤;
故選C.
點評 本題考查原電池與電解池的基礎知識,正確判斷正負極、陰陽極,注意電極反應式的書寫及電子轉移的計算,正確判斷化合價的變化為解答該題的關鍵,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| 選項 | 性質 | 實際應用 |
| A | MgO熔點高 | 可用作耐火材料 |
| B | KMnO4具有強氧化性 | 可用于漂白織物 |
| C | 常溫下,鐵能被濃硫酸鈍化 | 常溫下,可用鐵質器皿盛放濃硫酸 |
| D | TiCl4在水中能發生水解 | 可用TiCl4溶液制備TiO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| 物質 | 雜質 | 試劑或用品 | 主要操作 | |
| A | 淀粉 | 碘化鉀 | 半透膜 | 滲析 |
| B | Fe(NO3)2 | Ba(NO3)2 | 硫酸 | 過濾 |
| C | Fe | I2 | / | 加熱 |
| D | 溴 | 四氧化碳 | 蒸餾裝置 | 蒸餾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
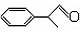 )曾入選倫敦奧運會指定產品,下面是工業合成龍葵醛的路線圖(部分反應條件及副產物已略去),回答問題:
)曾入選倫敦奧運會指定產品,下面是工業合成龍葵醛的路線圖(部分反應條件及副產物已略去),回答問題: $→_{催化劑}^{CH_{3}CH=CH_{2}}$$\stackrel{A}{{C}_{9}{H}_{12}}$$→_{光照}^{Cl_{2}}$$\stackrel{B}{{C}_{9}{H}_{11}{C}_{1}}$→${\stackrel{C}{{C}_{9}{H}_{10}}}_{\;}$$\stackrel{HBr}{→}$$\stackrel{D}{{C}_{9}{H}_{11}Br}$→$\stackrel{E}{{C}_{9}{H}_{12}O}$$→_{△}^{催化劑}$龍葵醛
$→_{催化劑}^{CH_{3}CH=CH_{2}}$$\stackrel{A}{{C}_{9}{H}_{12}}$$→_{光照}^{Cl_{2}}$$\stackrel{B}{{C}_{9}{H}_{11}{C}_{1}}$→${\stackrel{C}{{C}_{9}{H}_{10}}}_{\;}$$\stackrel{HBr}{→}$$\stackrel{D}{{C}_{9}{H}_{11}Br}$→$\stackrel{E}{{C}_{9}{H}_{12}O}$$→_{△}^{催化劑}$龍葵醛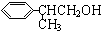 +O2
+O2
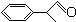 +2H2O.
+2H2O. 或
或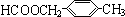 (任寫一種).
(任寫一種).查看答案和解析>>
科目:高中化學 來源: 題型:解答題
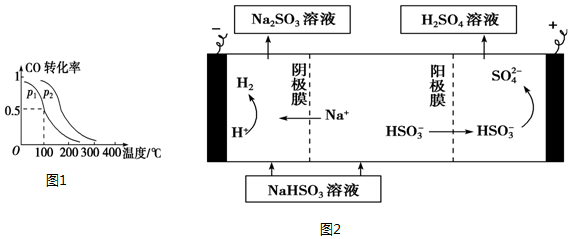
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2.0gH218O與D216O的混合物中所含中子數為NA | |
| B. | 0.1molCl2溶于足量水中,轉移的電子數為0.1NA | |
| C. | 常溫常壓下50g 46%的乙醇溶液中,所含氧原子數目為0.5NA | |
| D. | 25℃時,pH=13的Ba(OH)2溶液中含有的OH-數目為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 生活污水使用明礬殺菌消毒 | B. | 向燃煤中加入適量石灰石“固硫” | ||
| C. | 推廣使用可降解塑料防止白色污染 | D. | 提倡公交出行可減少氮氧化物排放 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 性質 | 實際應用 |
| A | 活性炭可吸附水中的懸浮物 | 用于自來水的殺菌消毒 |
| B | SO2具有還原性 | 漂白紙漿 |
| C | 鐵被氧氣氧化時會放出熱量 | 鐵、活性炭、無機鹽、水等的混合物制成暖寶貼 |
| D | 氧化鋁是兩性氧化物 | 作耐高溫材料 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com