
目前高鐵酸鈉(Na2FeO4)被廣泛應用于水處理,具有高效、無毒的優點。
(1)在處理水的過程中,Na2FeO4起到殺菌、消毒、凈水的作用,請說明應用了Na2FeO4的哪些性質:__________________________________________________________________________
(2) 某地海水樣品經Na2FeO4處理后,所含離子及其濃度如下表所示(H+和OH-未列出):
| 離子 | SO | Mg2+ | Fe3+ | Na+ | Cl- |
| 濃度(mol/L) | a | 0.05 | 0.10 | 0.50 | 0.58 |
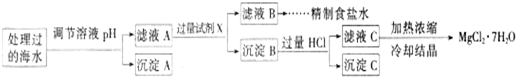
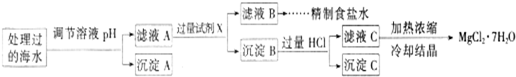
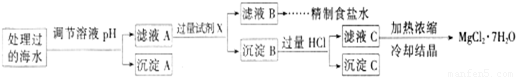
常溫下,取一定量經Na2FeO4處理過的海水為原料制備精制食鹽水和MgCl2·7H2O,過程如下:

Ksp[Fe(OH)3]=1.0×10-38;Ksp[Mg(OH)2]=5.0×10-12;操作過程中溶液體積的變化忽略不計。
① 表格中的a________0.16(填“<”、“>”或“=”)。
② 沉淀A的組成為________(填化學式);在調節溶液pH時,理論上應調節的pH的范圍是________。
③ 加入的過量試劑X為____________________(填化學式)。
④ 加入過量HCl的作用為_________________________________________________。
 舉一反三單元同步過關卷系列答案
舉一反三單元同步過關卷系列答案科目:高中化學 來源: 題型:
| 離子 | SO42- | Mg2+ | Fe3+ | Na+ | Cl- |
| 濃度(mol/L) | a | 0.05 | 0.10 | 0.50 | 0.58 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 離子 | SO42- | Mg2+ | Fe3+ | Na+ | Cl- |
| 濃度(mol/L) | a | 0.05 | 0.10 | 0.50 | 0.58 |
查看答案和解析>>
科目:高中化學 來源:河北省模擬題 題型:填空題



 ;操作過程中溶液體積的變化忽略不計。
;操作過程中溶液體積的變化忽略不計。 查看答案和解析>>
科目:高中化學 來源:2012-2013學年遼寧省本溪一中高三(上)第三次月考化學試卷(解析版) 題型:解答題
| 離子 | SO42- | Mg2+ | Fe3+ | Na+ | Cl- |
| 濃度(mol/L) | a | 0.05 | 0.10 | 0.50 | 0.58 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com