
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 | |
| 第2周期 | ① | ② | ③ | |||||
| 第3周期 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 第4周期 | ⑨ | ⑩ |
分析 由元素在周期表的位置可知,①~⑩元素分別為C、N、O、Mg、Al、S、Cl、Ar、K、Ca;
(1)由上述分析可知元素的名稱;
(2)K的金屬性最強,N的氣態氫化物能與其最高價氧化物對應的水化物發生反應生成鹽為銨鹽;
(3)利用氫化物的穩定性、與變價金屬反應、最高價含氧酸等比較非金屬性;
(4)設計成原電池,Al在負極失去電子生成偏鋁酸根離子.
解答 解:由元素在周期表的位置可知,①~⑩元素分別為C、N、O、Mg、Al、S、Cl、Ar、K、Ca;
(1)元素的名稱⑧為氬氣,⑩為鈣,故答案為:氬;鈣;
(2)在①~⑩元素中,金屬性最強的元素是K,氣態氫化物能與其最高價氧化物對應的水化物發生反應生成鹽的元素是N,故答案為:K;N;
(3)a.常溫下⑥的單質和⑦的單質狀態不同,為物理性質,不能比較非金屬性,故不選
b.⑦的氫化物比⑥的氫化物穩定,可知非金屬性,故選;
c.一定條件下⑥和⑦的單質都能與氫氧化鈉溶液反應,為物質的特性,不能比較非金屬性,故不選;
d.一定條件下⑥和⑦的單質與Fe反應的產物不同,可知得電子的難易,故選;
故答案為:bd;
(4)⑤的單質可以與⑨的最高價氧化物的水化物的溶液反應,若將該反應設計成原電池,其負極的電極反應式為Al-3e-+4OH-=AlO2-+2H2O,故答案為:Al-3e-+4OH-=AlO2-+2H2O.
點評 本題考查位置、結構與性質,為高頻考點,把握元素的位置、性質、元素周期律為解答的關鍵,側重分析與應用能力的考查,題目難度不大.


 小學教材全測系列答案
小學教材全測系列答案 小學數學口算題卡脫口而出系列答案
小學數學口算題卡脫口而出系列答案 優秀生應用題卡口算天天練系列答案
優秀生應用題卡口算天天練系列答案科目:高中化學 來源: 題型:解答題
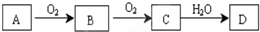
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | B | ||||||
| 2 | D | E | F | G | ||||
| 3 | C | H | I |
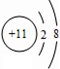 ,I的原子結構示意圖
,I的原子結構示意圖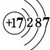 .
.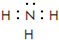 ;該物質溶于水后的溶液呈堿性(填“酸”、“堿”或“中”).
;該物質溶于水后的溶液呈堿性(填“酸”、“堿”或“中”).查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
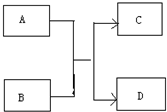 運用有關知識,回答下列問題.
運用有關知識,回答下列問題.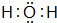 ,實驗室中檢驗C的試劑及現象是濕潤的紅色石蕊試紙變藍色.
,實驗室中檢驗C的試劑及現象是濕潤的紅色石蕊試紙變藍色.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
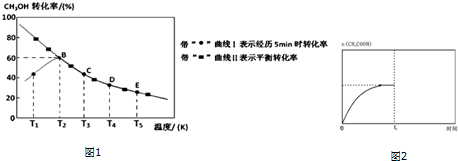
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 蔗糖變黑體現了濃硫酸的脫水性 | |
| B. | 蔗糖體積膨脹變成疏松多孔的海綿狀物質炭 | |
| C. | 實驗中有大量氣體產生體現了濃硫酸的強酸性 | |
| D. | 將產生的氣體通入品紅溶液,溶液會褪色 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com