
【題目】工業上用菱錳礦(MnCO3)[含FeCO3、SiO2、Cu2(OH)2CO3等雜質]為原料制取二氧化錳,其流程示意圖如下:
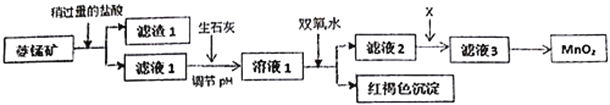
已知:生成氫氧化物沉淀的pH
Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
開始沉淀時 | 8.3 | 6.3 | 2.7 | 4.7 |
完全沉淀時 | 9.8 | 8.3 | 3.7 | 6.7 |
Ksp(CuS)=6.3×10-16 Ksp(MnS)= 3×10-14
注:金屬離子的起始濃度為0.1 mol/L
回答下列問題:
(1)含雜質的菱錳礦使用前需將其粉碎,主要目的是_________________________。濾渣1的成分是_________,鹽酸溶解MnCO3的離子方程式是_________________________________;
(2)用生石灰而不用NaOH調節pH的原因是_______________________________;
(3)濾液2中加入某種物質X可以除去Cu2+,最適合的是_______________;
A.MnO2 B.NaOH C.MnS
該反應的離子方程式是____________________________;
(4)將MnCl2轉化為MnO2的一種方法是將酸化的NaClO3溶液氧化Mn2+,請補充并配平下列方程;____Mn2++_____ClO3-+______=____Cl2↑+____MnO2+_________;_________________
(5)將MnCl2轉化為MnO2的另一種方法是電解法。(填“正極”或“負極”或“陰極”或“陽極”)
① MnO2在電解池的__________________(填“正極”或“負極”或“陰極”或“陽極”)生成;
② 若直接電解MnCl2溶液,生成MnO2的同時會產生少量Cl2。檢驗Cl2的操作是_______________。
【答案】 增大反應物接觸面積,提高反應速率 SiO2 MnCO3+2H+=Mn2++CO2↑+H2O 生石灰經濟實惠 C MnS+Cu2+=Mn2++CuS 5 2 4H2O 1 5 8H+ 陽極 將潤濕的淀粉碘化鉀試紙置于陽極附近,若試紙變藍則證明有Cl2生成
【解析】本題主要考查對于制取二氧化錳工藝流程的評價。
(1)含雜質的菱錳礦使用前需將其粉碎,主要目的是增大反應物接觸面積,提高反應速率。濾渣1的成分是不溶于鹽酸的SiO2,鹽酸溶解MnCO3的離子方程式是MnCO3+2H+=Mn2++CO2↑+H2O;
(2)用生石灰而不用NaOH調節pH的原因是生石灰經濟實惠;
(3)濾液2中加入某種物質X可以除去Cu2+,最適合的是C;因A.無效,B.帶來雜質離子Na+,C.合適,故選C。該反應的離子方程式是MnS+Cu2+=Mn2++CuS;
(4)根據電子守恒初步將方程式配平為5Mn2++2ClO3-+______=Cl2↑+5MnO2+_________, 再根據電荷守恒和元素守恒得完整方程式:5Mn2++2ClO3-+4H2O =Cl2↑+5MnO2+8H+;
(5)①MnO2是氧化產物,在電解池的陽極生成;
②檢驗Cl2的操作是將潤濕的淀粉碘化鉀試紙置于陽極附近,若試紙變藍則證明有Cl2生成。


 小天才課時作業系列答案
小天才課時作業系列答案 一課四練系列答案
一課四練系列答案 黃岡小狀元滿分沖刺微測驗系列答案
黃岡小狀元滿分沖刺微測驗系列答案 新輔教導學系列答案
新輔教導學系列答案 陽光同學一線名師全優好卷系列答案
陽光同學一線名師全優好卷系列答案科目:高中化學 來源: 題型:
【題目】電解硫酸鈉溶液聯合生產硫酸和燒堿溶液的裝置如圖所示,其中陰極和陽極均為惰性電極.測得同溫同壓下,氣體甲與氣體乙的體積比約為1:2,以下說法不正確的是( ) 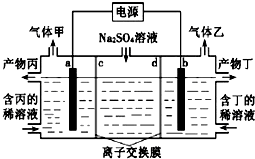
A.a極與電源的正極相連
B.產物丙為硫酸溶液
C.離子交換膜d為陽離子交換膜(允許陽離子通過)
D.a電極反應式為2H2O+2e﹣═2OH﹣+H2↑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NH4Al(SO4)2是食品加工中最為快捷的食品添加劑,用于焙烤食品中;NH4HSO4在分析試劑、醫藥、電子工業中用途廣泛.請回答下列問題: 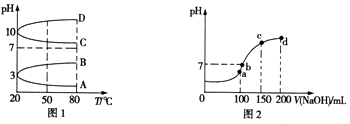
(1)相同條件下,相等濃度的NH4Al(SO4)2溶液中c(NH4+)NH4HSO4溶液中c(NH4+) (填“=”、“>”或“<”).
(2)如圖1是0.1molL﹣1電解質溶液的pH隨溫度變化的圖象. ①其中符合0.1molL﹣1 NH4Al(SO4)2的pH隨溫度變化的曲線是(填寫字母).
②室溫時,0.1molL﹣1 NH4Al(SO4)2溶液中2c(SO42﹣)﹣c(NH4+)﹣3c(Al3+)=molL﹣1(填
計算式).
(3)室溫時,向100mL 0.1molL﹣1 NH4HSO4溶液中滴加0.1molL﹣1NaOH溶液,得到溶液的pH與NaOH溶液體積的關系曲線如圖2所示.圖中a、b、c、d四個點,水的電離程度最大的是;在b點,溶液中各離子濃度由大到小的順序是 .
(4)電解制備Al(OH)3時,電極分別為Al片和石墨,電解質溶液為Na2CO3溶液,電解總反應的方程式為 .
(5)一種可超快充電的新型鋁電池,充放電時AlCl4﹣和Al2Cl7﹣兩種離子在Al電極上相互轉化,其他離子不參與電極反應,放電時負極Al的電極反應式為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某興趣小組用題圖1裝置(夾持裝置略)收集某葡萄酒中SO2 , 并對含量進行測定. 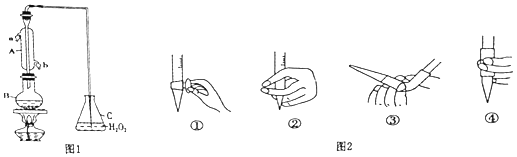
(1)儀器A的名稱是 .
(2)B中加入300.00mL葡萄酒和適量鹽酸,加熱使SO2全部逸出并與C中H2O2完全反應,其化學方程式為 .
(3)除去C中過量的H2O2 , 然后用0.0900mol/LNaOH標準溶液進行滴定,滴定前排氣泡時,應選擇圖2中的 .
(4)若滴定終點時溶液的pH=8.8,則選擇的指示劑為 .
(5)該測定結果往往比實際值偏高,分析是由于采用試劑不當引起的,可能的原因為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以下說法正確的是
A.C60與金剛石一樣屬于原子晶體
B.由非金屬元素組成的化合物不一定是共價化合物
C.分子晶體中必含化學鍵
D.干冰升華破壞了共價鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以天然氣為原料合成甲醇,有關熱化學方程式如下:
①2CH4(g)+O2(g)==2CO(g)+4H2(g) △H1=-70.8kJmol-1
②CO(g)+2H2(g)![]() CH3OH(g) △H2
CH3OH(g) △H2
③2CH4(g)+O2(g)![]() 2CH3OH(g) △H3=-251.0 kJmol-1
2CH3OH(g) △H3=-251.0 kJmol-1
(1)反應②的△H2=________kJmol-1;
(2)在體積可變的密閉在器中投入1 mol CO和2 mol H2,在不同條件下發生反應:CO(g)+2H2(g)![]() CH3OH(g)。實驗測得平衡時CH3OH的物質的量隨溫度、壓強變化如圖1所示。
CH3OH(g)。實驗測得平衡時CH3OH的物質的量隨溫度、壓強變化如圖1所示。

①M 點時,H2 的轉化率為_________;壓強: p1_______(填“>”“<”或“=”)p2;
②反應速率:N 點v正(CO) _______(填“>”“<”或“=”)M 點v 逆(CO)
③若壓強為p1、在1L恒容密閉容器中進行上述反應(起始投料不變),在不同溫度下上述反應的平衡常數的對數(IgK)如圖2所示。則溫度為506K時,平衡常數K=____________, B、C、D、E四點中能正確表示該反應的1gK 與T的關系的點為________________。
④若在2L恒容密閉容器中充入x (x>0)mol H2、2 mol CO、和8 mol CH3OH(g),在 506 K下進行上述反應。為了使該反應逆向進行,x的范圍為________________。
(3)某甲醇-空氣燃料電池以KOH溶液為電解質溶液。當KOH全部轉化成KHCO3時停止放電,寫出此時負極的電極反應式______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.被譽為改變未來世界的十大新科技之一的燃料電池。 右圖為氫氧燃料電池的結構示意圖,電解質溶液為KOH溶液,電極材料為疏松多孔石墨棒.當氧氣和氫氣分別連續不斷地從正、負兩極通入燃料電池時,便可在閉合回路中不斷地產生電流.

試回答下列問題:
(1)燃料電池的優點是________;電解質溶液中的OH-移向______極(填“負”或“正”).
(2)寫出氫氧燃料電池工作時正極反應式:_______________________。
(3)若將此燃料電池改進為直接以甲烷和氧氣為原料進行工作時,負極反應式為___________.
(4)利用該裝置可以處理氮的氧化物和NH3 尾氣,總反應為:6NO2 +8NH3=7N2+12H2O,負極反應式為__________。
II.將鋅片和銀片浸入稀硫酸中組成原電池,若該電池中兩電極的總質量為80 g,工作一段時間后,取出鋅片和銀片洗凈干燥后稱重,總質量為41g,試計算:
(1)產生氫氣的體積(標準狀況)為________________;
(2)通過導線的電子數為__________(用NA表示).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示是幾種常見的化學電源示意圖,有關說法不正確的是( ) 
A.上述電池分別屬于一次電池、二次電池和燃料電池
B.干電池在長時間使用后,鋅筒被破壞
C.氫氧燃料電池是一種具有應用前景的綠色電源
D.鉛蓄電池工作過程中,每通過 2 mol 電子,負極質量減輕 207 g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】微生物燃料電池是指在微生物的作用下將化學能轉化為電能的裝置。某微生物燃料電池的工作原理如圖所示,下列說法正確的是

A. HS-在硫氧化菌作用下轉化為SO42-的反應為:HS-+4H2O-8e-== SO42-+9H+
B. 電子從b流出,經外電路流向a
C. 如果將反應物直接燃燒,能量的利用率不會變化
D. 若該電池電路中有0.4mol電子發生轉移,則有0.5molH+通過質子交換膜
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com