
分析 由①實驗可知,向第一份溶液中加入AgNO3溶液,有白色沉淀產生,白色沉淀為AgCl或碳酸銀、硫酸銀;
由②可知,向第二份溶液中加入足量NaOH 溶液后加熱,收集到氣體為氨氣,其物質的量為0.02mol,原溶液中一定含NH4+;
由③可知,在甲溶液中通入過量CO2,生成白色沉淀,沉淀經過濾、洗滌、灼燒,質量為1.02g,氧化鋁的物質的量為$\frac{1.02g}{102g/mol}$=0.01mol,原溶液含Al3+為0.02mol,且原溶液不含Fe3+、Mg2+,含鋁離子時不含CO32-;
由④第三份加足量BaCl2溶液后,得白色沉淀,沉淀經足量鹽酸洗滌、干燥后,質量為11.65g,沉淀為硫酸鋇,物質的量為$\frac{11.65g}{233g/mol}$=0.05mol,原溶液中含SO42-為0.05mol,且原溶液不含Ba2+,結合離子共存、電荷守恒解答.
解答 解:由①實驗可知,向第一份溶液中加入AgNO3溶液,有白色沉淀產生,白色沉淀為AgCl或碳酸銀、硫酸銀;
由②可知,向第二份溶液中加入足量NaOH 溶液后加熱,收集到氣體為氨氣,其物質的量為0.02mol,原溶液中一定含NH4+;
由③可知,在甲溶液中通入過量CO2,生成白色沉淀,沉淀經過濾、洗滌、灼燒,質量為1.02g,氧化鋁的物質的量為$\frac{1.02g}{102g/mol}$=0.01mol,原溶液含Al3+為0.02mol,且原溶液不含Fe3+、Mg2+,含鋁離子時不含CO32-;
由④第三份加足量BaCl2溶液后,得白色沉淀,沉淀經足量鹽酸洗滌、干燥后,質量為11.65g,沉淀為硫酸鋇,物質的量為$\frac{11.65g}{233g/mol}$=0.05mol,原溶液中含SO42-為0.05mol,且原溶液不含Ba2+,
由電荷守恒可知,0.02×1+0.02×3<0.05×2,可知一定含陽離子K+,不能確定是否含Cl-,
(1)一定存在K+、Al3+、NH4+、SO42-,不存在的離子是Fe3+、Mg2+、Ba2+、CO32-,不能確定是否存在的離子是Cl-,
故答案為:Fe3+、Mg2+、Ba2+、CO32-;Cl-;
(2)溶液中肯定存在的陰離子為SO42-,其濃度為$\frac{0.05mol}{0.1L}$=0.5mol/L,故答案為:SO42-;0.5mol/L;
(3)由電荷守恒可知,含Al3+、NH4+、SO42-,陽離子電荷總數小于陰離子電荷總數,則一定含K+,故答案為:是;陽離子電荷總數小于陰離子電荷總數.
點評 本題考查無機物的推斷,為高頻考點,把握離子之間的反應、現象、離子檢驗方法為解答的關鍵,側重分析與推斷能力的考查,注意電荷守恒的應用,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 2p能級上只有1個空軌道的原子和3p能級上只有1個空軌道的原子 | |
| B. | 最外層電子排布為3s2的原子和最外層電子排布為4s2的原子 | |
| C. | 最外層電子排布為ns2的原子和最外層電子排布為ns2np6的原子 | |
| D. | 2p能級上有2個未成對電子的原子和3p能級上有2個未成對電子的原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
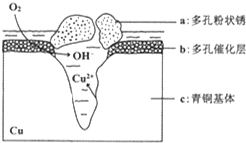 銅是一種重要的有色金屬,近年來用途越來越廣泛.請回答下列問題:
銅是一種重要的有色金屬,近年來用途越來越廣泛.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2.0 mol/L | B. | 0.6 mol/L | C. | 1.7 mol/L | D. | 1.2 mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 組合序號 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ |
| 組合數據 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 元素第一電離能大小:J>R>Q | |
| B. | 含T元素的兩種鹽的溶液,一定不能相互反應 | |
| C. | Z的含氧酸一定為強酸 | |
| D. | Q、R、J三元素中J的電負性最大 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 溫度 | 283K | 293K | 303K |
| 溶解度(g/100g H2O) | 2.5 | 3.9 | 5.6 |
| 實驗步驟 | 預期現象和結論 |
| 步驟1:取適量試劑于潔凈燒杯中,加入足量蒸餾水,充分攪拌,靜置,過濾,得濾液和沉淀. | |
| 步驟2:取適量濾液于試管中,滴加稀硫酸. | 出現白色沉淀,說明該試劑中有Ba2+存在 |
| 步驟3:取適量步驟1中的沉淀于試管中,滴加稀鹽酸連接帶塞導氣管將產生的氣體導入澄清石灰水中. | 澄清石灰水變混濁.說明該試劑中含有BaCO3 |
| 步驟4:取步驟1中的濾液于燒杯中,用pH計測其pH值 | pH值明顯大于9.6,說明該試劑中含有Ba(OH)2. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④⑥ | B. | ②⑤⑥ | C. | ①②③④ | D. | ④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com