
 化學在環境保護中起著十分重要的作用,催化反硝化法和電化學降解法可用于治理水中硝酸鹽的污染.
化學在環境保護中起著十分重要的作用,催化反硝化法和電化學降解法可用于治理水中硝酸鹽的污染.分析 (1)①氮氣分子中氮原子間形成3個共用電子對;
②在催化劑條件下,氫氣和硝酸根離子發生氧化還原反應生成氮氣、水和氫氧根離子;先根據溶液pH的變化計算氫氧根離子反應速率,再根據氫氧根離子和硝酸根離子之間的關系式計算硝酸根離子反應速率;
(2)①由圖示知在Ag-Pt電極上NO3-發生還原反應,因此Ag-Pt電極為陰極,則B為負極,A為電源正極;陰極反應是NO3-得電子發生還原反應生成N2,利用電荷守恒與原子守恒知有氫離子參與反應且有水生成;
②轉移2mol電子時,陽極(陽極反應為H2O失電子氧化為O2和H+)消耗1mol水,產生2molH+進入陰極室,陽極室質量減少18g;陰極室中放出0.2molN2(5.6g),同時有2molH+(2g)進入陰極室.
解答 解:(1)①N2分子中氮原子間通過氮氮三鍵結合,因此其結構式為N≡N,故答案為:N≡N;
②利用溶液pH變化可知有OH-生成,再結合原子守恒可寫出反應的離子方程式為2NO3-+5H2=N2+2OH-+4H2O,利用離子方程式知v(NO3-)=v(OH-)=$\frac{10{\;}^{-2}-10{\;}^{-7}}{10}$mol/(L•min)=0.001 mol/(L•min),
故答案為:2NO3-+5H2=N2+2OH-+4H2O;0.001;
(2)①由圖示知在Ag-Pt電極上NO3-發生還原反應,因此Ag-Pt電極為陰極,則B為負極,A為電源正極;在陰極反應是NO3-得電子發生還原反應生成N2,利用電荷守恒與原子守恒知有H+參與反應且有水生成,所以陰極上發生的電極反應式為:2NO3-+12H++10e-=N2+6H2O,
故答案為:A;2NO3-+12H++10e-=N2+6H2O;
②轉移2mol電子時,陽極(陽極反應為H2O失電子氧化為O2和H+)消耗1mol水,產生2molH+進入陰極室,陽極室質量減少18g;陰極室中放出0.2molN2(5.6g),同時有2molH+(2g)進入陰極室,因此陰極室質量減少3.6g,故膜兩側電解液的質量變化差(△m左-△m右)=18g-3.6g=14.4g,
故答案為:14.4.
點評 本題考查結構式和離子方程式的書寫、電解原理、反應速率計算、平衡移動等知識點,(2)中②要注意該題中陰極室有氫離子進入,易漏掉,為易錯點.


科目:高中化學 來源: 題型:選擇題

| A. | 該物質屬于烴類 | B. | 該物質易溶于水 | ||
| C. | 該物質能使酸性高錳酸鉀溶液褪色 | D. | 該物質是一種高分子化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 25℃,1.01×105 Pa,64g SO2中含有的原子數為3NA | |
| B. | 在1mol的Na2O2晶體中離子總數為3NA | |
| C. | 在0.5mol/L NaCl溶液中,含有的Na+數目為0.5NA | |
| D. | 標準狀況下,11.2LH2O 含有的分子數為0.5NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 化學式 | 摩爾質量/(g•mol-1) | 質量/g | 物質的量/mol | 分子或離子數 |
| H2SO4 | 4.9 | |||
| SO2 | 0.5 | |||
| OH- | 6.02×1024 | |||
| NH4+ | 6.02×1022 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗現象 | 實驗結論 | |
| 甲 | 在光照條件下,試管內氣體顏色變淺了;試管內壁上出現了油狀液滴. | CH4與Cl2在光照條件下 發生化學反應 |
| 乙 | 迅速剝開黑紙,立即觀察,試管內氣體顏色為黃綠色. | CH4與Cl2在無光照條件下不發生化學反應. |

 .
.

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(NH4+)相等的(NH4)2SO4溶液、NH4HSO4溶液和NH4Cl溶液中,溶質濃度大小關系是:c[(NH4)2SO4]<c[(NH4HSO4]<c(NH4Cl) | |
| B. | 欲除去CuCl2溶液中混有少量的FeCl3,可加入CuO | |
| C. | 0.2mol/L HCl溶液與等體積0.05mol/L Ba(OH)2溶液混合后,溶液的pH=1 | |
| D. | 0.2mol/L的NaHCO3溶液中c(H+)+c(H2CO3)=c(CO32-)+c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
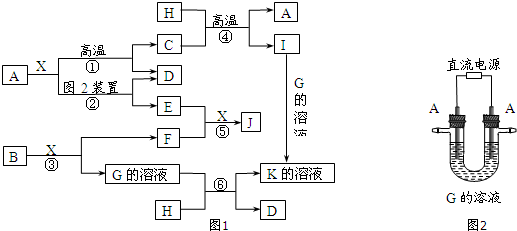
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 混合氣體的體積恒定不變 | |
| B. | 混合氣體的顏色不再改變 | |
| C. | 混合氣體的平均摩爾質量不變 | |
| D. | I2在混合氣體中的體積分數與H2在混合氣體中的體積分數相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com