
| A. | 一定溫度下,在恒容密閉容器中充入等體積的X、Y氣體,發生反應X(g)+Y(g)?2Z(g),一段時間后達到平衡,其他條件不變,再充入0.3mol Z,平衡時Y的體積分數增大 | |
| B. | 堿性鋅錳干電池工作過程中,每通過2mol電子,負極質量減輕130g | |
| C. | 通過測定CH3COONa溶液和NaHS溶液的pH,可以比較醋酸和氫硫酸酸性的強弱 | |
| D. | 將MgCl2、Mg(OH)2、MgCO3三種物質與水混合,加熱、灼燒,最終的固體產物相同 |
分析 A.再通入0.2 mol Z,等效為在原平衡基礎上增大壓強,反應前后氣體的體積不變,平衡不移動;
B.原電池中,Zn失電子作負極,負極反應式為Zn-2e-+2OH-═Zn(OH)2,MnO2得電子為正極,正極反應式為2MnO2+H2O+2e-=Mn2O3+2OH-;
C.Na2S對應的酸是HS-而不是H2S,應該根據等物質的量濃度的 CH3COONa和NaHS溶液pH比較CH3COOH和H2S的酸性強弱;
D.氯化鎂溶液蒸干得到水解產物,灼燒得到氧化鎂,氫氧化鎂蒸干灼燒得到氧化鎂,碳酸鎂溶液加熱得到氫氧化鎂,灼燒得到氧化鎂;
解答 解:A.因該反應前后氣體的體積不變,其他條件不變,再充入0.2 mol Z,平衡等效,Y的體積分數不變,故A錯誤;
B.根據電池反應Zn(s)+2MnO2(s)+H2O(l)﹦Zn(OH)2(s)+Mn2O3(s),消耗1mol的金屬鋅,轉移電子是2mol,所以當外電路中每通過2mol電子,消耗金屬鋅1mol,鋅的質量理論上減小1mol×65g/mol=65g,故B錯誤;
C.Na2S對應的酸是HS-而不是H2S,應該根據等物質的量濃度的 CH3COONa和NaHS溶液pH比較CH3COOH和H2S的酸性強弱,故C錯誤;
D.氯化鎂溶液蒸干得到水解產物,灼燒得到氧化鎂,氫氧化鎂蒸干灼燒得到氧化鎂,碳酸鎂溶液加熱得到氫氧化鈉,灼燒得到氧化鎂,將表中三種物質與水混合,加熱、灼燒,最終所得的固體產物相同,故D正確;
故選D.
點評 本題考查了化學平衡影響因素、原電池原理分析、鹽類水解原理應用等知識點,注意知識的熟練掌握和積累,題目難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 濃硫酸具有吸水性,因而能使蔗糖炭化 | |
| B. | 濃硫酸在常溫下能迅速與銅片反應放出二氧化硫氣體 | |
| C. | 濃硫酸是一種干燥劑,能干燥二氧化硫、氫氣、氨氣等氣體 | |
| D. | 濃硫酸在常溫下能夠使鐵、鋁表面形成氧化膜而鈍化 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
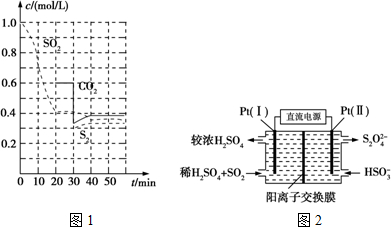
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Kb | B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$ | C. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$ | D. | n(NH4+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 左盤下沉 | B. | 右盤下沉 | C. | 仍保持平衡 | D. | 無法判斷 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 單質的沸點:A>B | B. | B與C不能存在于同一離子化合物中 | ||
| C. | 氧化物的水化物的酸性:C<D | D. | 陰離子的半徑:C>D |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
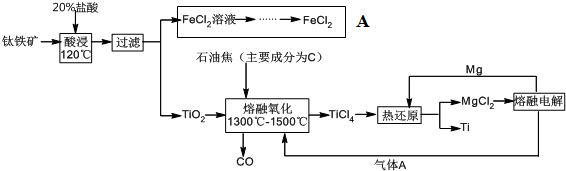
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ba(OH)2 溶液 | B. | NaOH溶液 | C. | BaCl2溶液 | D. | AgNO3溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com