
分析 (1)pH=5的NaHSO4溶液中,水的電離c(H+)=10-9mol/L,pH=9的NH3•H2O中水的電離c(H+)=10-9mol/L;
(2)等體積等物質的量濃度的NaHSO4與氨水混合后,反應生成硫酸鈉、硫酸銨,銨根離子水解顯酸性;PH=7,由電荷守恒分析離子濃度關系;用硫酸氫鈉與氫氧化鋇溶液制取硫酸鋇,硫酸根離子完全沉淀,則二者以1:2反應,生成硫酸鋇、NaOH;
(3)常溫下,a mL pH=3的鹽酸與b mL pH=11的氨水混合,充分反應.若a=b,反應后一水合氨又電離出氫氧根離子,溶液呈堿性;
(4)①溶液中溶質濃度相同,氫氧化鈉是強堿,電離產生氫氧根離子,pH最大,鹽中陽離子相同,酸越弱,其鹽的酸根水解程度越大,據此解答.
②根據是否存在平衡分析判斷,不存在平衡的pH值變化大;
③碳酸根、碳酸氫根與鋁離子發生徹底雙水解反應生成氫氧化鋁與二氧化碳;
④HCO3-、AlO2-之間反應.
解答 解:(1)pH=5的NaHSO4溶液中,水的電離c(H+)=10-9mol/L,pH=9的NH3•H2O中水的電離c(H+)=10-9mol/L,則兩溶液中水的電離程度相等,
故答案為:=;
(2)等體積等物質的量濃度的NaHSO4與氨水混合后,反應生成硫酸鈉、硫酸銨,銨根離子部分水解溶液顯酸性,水解離子反應為:NH4++H2O?NH3•H2O+H+;
pH=7,氫離子與氫氧根離子濃度相等,由電荷守恒可知離子濃度關系為:c(Na+)+c(NH4+)=2c(SO42-);
用硫酸氫鈉與氫氧化鋇溶液制取硫酸鋇,硫酸根離子完全沉淀,則二者以1:2反應,生成硫酸鋇、NaOH,溶液顯堿性,溶液的pH>7,
故答案為:NH4++H2O?NH3•H2O+H+;=;>;
(3)常溫下,a mL pH=3的鹽酸與b mL pH=11的氨水混合,充分反應.若a=b,反應后一水合氨又電離出氫氧根離子,溶液呈堿性,溶液中電荷守恒分析,離子濃度的關系為:c(NH4+)>c(Cl-)>c(OH-)>c(H+);
故答案為:c(NH4+)>c(Cl-)>c(OH-)>c(H+);
(4)①.①、②、③、④是鹽,⑤是堿,濃度相同,堿的PH值最大,①、②、③、④四種鹽的陽離子相同,其陰離子對應的酸越弱,酸根的水解程度越大,酸性:醋酸>碳酸>碳酸氫根>偏鋁酸,濃度相同,酸根的水解程度越大,pH值越大,故pH為④<②<①<③<⑤,故答案為:④<②<①<③<⑤.
②.①②③④都存在水解平衡,當稀釋時,鹽的弱酸根又水解出部分離子進行補充;氫氧化鈉是強堿,完全電離,不存在電離平衡,所以當稀釋時,其pH變化最大;
故答案為:⑤;
③碳酸根、碳酸氫根與鋁離子發生徹底雙水解反應生成氫氧化鋁與二氧化碳,NaAlO2與氯化鋁發生雙水解反應生成氫氧化鋁沉淀,CH3COONa與氯化鋁不反應,NaOH與氯化鋁反應生成氫氧化鋁沉淀,故答案為:①②;
④NaHCO3、NaAlO2的陰離子之間能反應,即HCO3-+AlO2-+H2O═Al(OH)3↓+CO32-,故答案為:HCO3-+AlO2-+H2O═Al(OH)3↓+CO32-.
點評 本題考查了溶液中的離子濃度大小比較,題目難度中等,試題涉及鹽類水解、電離、離子之間的反應等知識點,綜合性較強,充分考查了學生靈活應用基礎知識的能力.


 百年學典課時學練測系列答案
百年學典課時學練測系列答案 仁愛英語同步練習冊系列答案
仁愛英語同步練習冊系列答案科目:高中化學 來源: 題型:選擇題
| A. | 纖維素 滌綸 | B. | 麥芽糖 胰島素 | ||
| C. | 聚乙烯 酚醛樹脂 | D. | 淀粉 聚異戊二烯 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
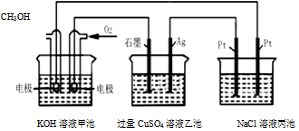
| A. | 甲池是電能轉化為化學能的裝置,乙、丙池是化學能轉化電能的裝置 | |
| B. | 甲池通入CH3OH的電極反應為CH3OH-6e-+2H2O═CO32-+8H+ | |
| C. | 甲池中消耗280mL(標準狀況下)O2,此時乙池中銀極增重1.6g | |
| D. | 反應一段時間后,向丙池中加入一定量鹽酸,一定能使NaCl溶液恢復到原濃度 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2.25mol/L | B. | 2mol/L | C. | 4mol/L | D. | 0.6mol/L |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com