
隨著化石能源的大量開采以及污染的加劇,污染氣體的治理和開發利用日益迫切。
(1)Bunsen熱化學循環制氫工藝由下列三個反應組成;
SO2(g) + I2(g) + 2H2O(g) = 2HI(g) + H2SO4(l) ∆H=a kJ/mol ①
2H2SO4(l) = 2H2O(g) + 2SO2(g) + O2(g) ∆H= b kJ/mol ②
2HI(g) = H2(g) + I2(g) ∆H= c kJ/mol ③
則2H2O(g) = 2H2(g) + O2(g) ∆H= kJ/mol
(2)CO2 和CH4 是兩種重要的溫室氣體,以表面覆蓋有Cu2Al2O4 的二氧化鈦為催化劑。可以將CO2 和CH4直接轉化為乙酸。

①不同溫度下催化劑的催化效率與乙酸的生成速率如圖Ⅰ所示,該反應體系應將溫度控制在 ℃左右。
②將Cu2Al2O4 溶解在稀硝酸中的離子方程式為 。
(3)甲醇(CH3OH)被稱為21世紀的新型燃料。在體積為V L的某反應容器中,a mol CO與2a mol H2 在催化劑作用下反應生成甲醇:CO(g) + 2H2(g)  CH3OH(g) ,CO的平衡轉化率與溫度的關系如圖Ⅱ所示:
CH3OH(g) ,CO的平衡轉化率與溫度的關系如圖Ⅱ所示:
①該反應是 (填“放熱”或“吸熱”)反應
②在其他條件不變的情況下,反應容器中再增加amol CO與2amolH2 ,達到新平衡時,CO的轉化率 (填“增大”、“減小”或“不變”)。
③100℃,反應CH3OH(g)  CO(g) + 2H2(g) 的平衡常數為 (用含有a、V的代數表示)。
CO(g) + 2H2(g) 的平衡常數為 (用含有a、V的代數表示)。
(4)某實驗小組設計了如圖III所示的甲醇燃料電池裝置。
①該電池工作時,OH- 向 (填“a”或“b”)極移動
②工作一段時間后,測得該溶液的pH減小,該電池負極反應的電極反應式為: 。
科目:高中化學 來源:2015-2016學年陜西西安長安一中高二下第二次月考化學卷(解析版) 題型:選擇題
扁桃酸衍生物是重要的醫藥中間體,以A和B 為原料合成扁桃酸衍生物F路線如下:
(1)A的分子式為C2H2O3,可發生銀鏡反應,且具有酸性,A所含官能團名稱為:_________,寫出A+B→C的化學反應方程式為_____________________.
(2) 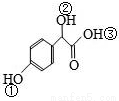 中①、②、③ 3個—OH的酸性有強到弱的順序是:__________。
中①、②、③ 3個—OH的酸性有強到弱的順序是:__________。
(3)E是由2分子C生成的含有3個六元環的化合物,寫出E的結構簡式_____________
(4)D→F的反應類型是_____________,1mol F在一定條件下與足量NaOH溶液反應,最多消耗NaOH的物質的量為______________mol
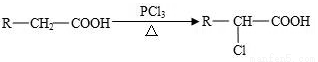
(5)已知:
A有多種合成方法,在方框中寫出由乙酸合成A的路線流程圖(其他原料任選)合成路線流程圖示例如下:
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江西省高一下第三次考試化學試卷(解析版) 題型:選擇題
對于反應A+B=C,下列條件的改變一定能使化學反應速率加快的是
A.增加A的物質的量 B.升高體系的溫度
C.減少C的物質的量 D.增加體系的壓強
查看答案和解析>>
科目:高中化學 來源:2016屆海南省高三全真模擬二化學試卷(解析版) 題型:選擇題
下列說法中正確的是
① 鈉在空氣中燃燒生成淡黃色的Na2O2 ② 常溫下鋁制容器可儲運濃硫酸或濃硝酸③ 鹽酸既有氧化性又有還原性 ④ Fe(OH)3、FeCl2、H2SiO3都不能直接用化合反應制備 ⑤ SO2能使酸性高錳酸鉀溶液褪色,所以它具有漂白性
A.②③ B.①②③ C.①②③④ D.①②③⑤
查看答案和解析>>
科目:高中化學 來源:2016屆海南省高三全真模擬二化學試卷(解析版) 題型:選擇題
化學與生產、生活密切相關.下列敘述正確的是
A.煤的干餾與石油的分餾均屬于化學變化
B.BaSO4在醫學上用作鋇餐,Ba2+對人體無毒
C.14C可用于文物的年代鑒定, 14C與 13C互為同素異形體
D.葡萄糖注射液不能產生丁達爾現象,不屬于膠體
查看答案和解析>>
科目:高中化學 來源:2016屆貴州省高三十二模理科化學試卷(解析版) 題型:選擇題
下列指定條件下描述正確的是( )
A.石灰乳中通入Cl2制漂白精的離子反應方程式為:4OH-+2Ca2++2Cl2=2Cl-+Ca(ClO)2↓+2H2O
B.NaHCO3中滴入少量Ba(OH)2溶液,其離子方程式正確的是:H++CO32-+Ba2++OH-=BaCO3↓+H2O
C.1.0 mol·L-1的KNO3溶液中H+、Fe2+、Cl-、SO42- 能大量共存。
D.pH=12的溶液中K+、Na+、CH3COO-、Br-能大量共存。
查看答案和解析>>
科目:高中化學 來源:2016屆廣西柳州鐵路一中高三5月月考理科化學試卷(解析版) 題型:簡答題
合金貯氫材料具有優異的吸收氫性能,在配合氫能的開發中起到重要作用
(1)一定溫度下,某貯氫合金(M)的貯氫過程如圖所示,縱軸為平衡時氫氣的壓強(p),橫軸表 示固相中氫原子與金屬原子的個數比(H/M)。在O
示固相中氫原子與金屬原子的個數比(H/M)。在O A段,氫溶解于M中形成固溶體MHx,隨著氫氣壓強的增大,H/M逐慚增大;在AB段,MHx與氫氣發生氫化反應生成氫化物MHy,氫化反應方程式為:zMHx(s)+ H
A段,氫溶解于M中形成固溶體MHx,隨著氫氣壓強的增大,H/M逐慚增大;在AB段,MHx與氫氣發生氫化反應生成氫化物MHy,氫化反應方程式為:zMHx(s)+ H (g)==zMHy(s) △H(Ⅰ);在B點,氫化反應結束,進一步增大氫氣壓強,H/M幾乎不變。反應(Ⅰ)中z=_____(用含x和y的代數式表示)。溫度為T1時,2g某合金4min內吸收氫氣240mL,吸氫速率v=______mL•g-1•min-1。反應的焓變△H(Ⅰ)_____0(填“>”“<”或“=”)
(g)==zMHy(s) △H(Ⅰ);在B點,氫化反應結束,進一步增大氫氣壓強,H/M幾乎不變。反應(Ⅰ)中z=_____(用含x和y的代數式表示)。溫度為T1時,2g某合金4min內吸收氫氣240mL,吸氫速率v=______mL•g-1•min-1。反應的焓變△H(Ⅰ)_____0(填“>”“<”或“=”)
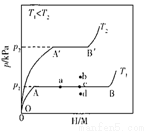
(2)η表示單位質量貯氫合金在氫化反應階段的最大吸氫量占其總吸氫量的比例,則溫度為T1、T2時,η(T1 )____ η(T2)(填“>”“<”或“=”)。當反應(Ⅰ)處于圖中a點時,保持溫度不變,向恒容體系中通入少量氫氣,達到平衡后反應(Ⅰ)可能處于圖中的_____點(填“b”“c”或“d”),該貯氫合金可通過________或________的方式釋放氫氣。
)____ η(T2)(填“>”“<”或“=”)。當反應(Ⅰ)處于圖中a點時,保持溫度不變,向恒容體系中通入少量氫氣,達到平衡后反應(Ⅰ)可能處于圖中的_____點(填“b”“c”或“d”),該貯氫合金可通過________或________的方式釋放氫氣。
(3)貯氫合金ThNi5可催化由CO、H 合成CH
合成CH 的反應,溫度為T時,該反應的熱化學方程式為_______ 。已知溫度為T時:CH
的反應,溫度為T時,該反應的熱化學方程式為_______ 。已知溫度為T時:CH (g)+2H2O=CO
(g)+2H2O=CO (g)+4H
(g)+4H (g) △H=+165KJ•mol?1
(g) △H=+165KJ•mol?1
CO(g)+H2O(g)=CO (g)+H
(g)+H (g) △H=-41KJ•mol?1
(g) △H=-41KJ•mol?1
查看答案和解析>>
科目:高中化學 來源:2016屆甘肅西北師大附中高三下第五次診斷理科化學試卷(解析版) 題型:選擇題
一種新型的乙醇電池,它用磺酸類質子溶劑。電池總反應為:C2H5OH+3O2 → 2CO2+3H2O,電池示意如圖,下列說法正確的是( )

A.a極為電池的正極
B.電池工作時電流由a極沿導線經燈泡再到b極
C.電池負極的電極反應為4H++O2+4e-== 2H2O
D.電池工作時,1mol乙醇被氧化時有12mol電子轉移
查看答案和解析>>
科目:高中化學 來源:2015-2016學年北大附中河南分校高一下期末化學試卷(解析版) 題型:選擇題
俄羅斯科學家在利用回旋加速器進行的實驗中,用含20個質子的鈣元素的同位素反復轟擊含95個質子的镅元素,結果成功制得4個第115號元素的原子。其與N元素同主族.這4個原子在生成數微秒后衰變成第113號元素.前者的一種核素為 。下列有關敘述正確的是( )
。下列有關敘述正確的是( )
A.115號元素衰變成113號元素是化學變化
B。115號元素X的近似相對原子質量為288
C.113號元素的原子最外層有3個電子
D.因115號元素與N元素同主族,所以是非金屬元素
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com