
【題目】一定條件下,對于恒容密閉容器中進行的可逆反應2NO2(g)![]() 2NO(g)+O2(g),下列說法中能說明反應一定已經達到化學平衡狀態的是( )
2NO(g)+O2(g),下列說法中能說明反應一定已經達到化學平衡狀態的是( )
①單位時間生成n mol O2的同時生成2n mol NO2;
②2v正(NO2)=v逆(O2)
③NO2、NO、O2的物質的量濃度之比為2:2:1;
④容器內壓強不再改變
⑤密閉容器中混合氣體的密度不再改變;
⑥混合氣體的平均相對分子質量不再改變
A.①④⑥B.②③⑤C.①②⑥D.①③⑤
【答案】A
【解析】
化學反應達到平衡狀態時,正逆反應速率相等,反應體系中各物質的物質的量不變、物質的量濃度不變、百分含量不變以及由此引起的一系列物理量不變,據此分析解答。
①中單位時間內生成n mol O2的同時生成2n mol NO2,正逆反應速率相等,說明反應已達到平衡狀態,故①正確;
②中兩物質的速率比與化學計量數比不同,不能判斷反應達平衡狀態,故②錯誤;
③中三種物質的濃度比在平衡時不一定為2:2:1,不能判斷反應達平衡狀態,故③錯誤;
④反應前后ΔV(g)≠0,壓強不變,意味著各物質的含量不再變化,說明已達到平衡狀態,故④正確;
⑤氣體體積固定、反應前后質量守恒,密度始終不變,不能據此判斷平衡狀態,故⑤錯誤;
⑥隨著反應的不斷進行,體系內的總物質的量不斷增大,當反應達平衡時,體系內總物質的量不再發生變化,體系內的平均相對分子質量不再發生變化,說明反應已達到平衡狀態,故⑥正確;
①④⑥正確,答案選A。


科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. 若H2O2分解產生1molO2,理論上轉移的電子數約為4×6.02×1023
B. 室溫下,pH=3的CH3COOH溶液與 pH=11的NaOH溶液等體積混合,溶液pH>7
C. 鋼鐵水閘可用犧牲陽極或外加電流的陰極保護法防止其腐蝕
D. 一定條件下反應N2+3H2![]() 2NH3達到平衡時,3v正(H2)=2v逆(NH3)
2NH3達到平衡時,3v正(H2)=2v逆(NH3)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組制取氯酸鉀和氯水并進行有關探究實驗。
實驗一 制取氯酸鉀和氯水
利用如圖所示的實驗裝置進行實驗。
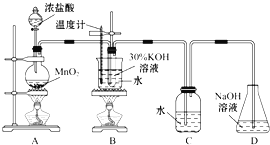
(1)制取實驗結束后,取出B中試管冷卻結晶,過濾,洗滌。該實驗操作過程需要的玻璃儀器有______。
(2)若對調B和C裝置的位置,_____(填“可能”或“不可能”)提高B中氯酸鉀的產率。
實驗二 氯酸鉀與碘化鉀反應的研究
(3)在不同條件下KClO3可將KI氧化為I2或KIO3。該小組設計了系列實驗研究反應條件對反應產物的影響,其中系列a實驗的記錄表如下(實驗在室溫下進行):
試管編號 | 1 | 2 | 3 | 4 |
0.20molL-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0molL-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
蒸餾水/mL | 9.0 | 6.0 | 3.0 | 0 |
實驗現象 |
①系列a實驗的實驗目的是______。
②設計1號試管實驗的作用是______。
③若2號試管實驗現象是溶液變為黃色,取少量該溶液加入______溶液顯藍色。
實驗三 測定飽和氯水中氯元素的總量
(4)根據下列資料,為該小組設計一個簡單可行的實驗方案(不必描述操作過程的細節):_____。
資料:①次氯酸會破壞酸堿指示劑;
②次氯酸或氯水可被SO2、H2O2和FeCl2等物質還原成Cl-。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中不正確的是( )
A. 乙烯與苯都能使溴水褪色,但褪色原理不同
B. 1 mol乙烯與Cl2完全加成,然后與Cl2發生取代反應,共消耗氯氣 5mol
C. 溴水遇到乙醛溶液出現褪色現象,是因為發生了氧化反應
D. ![]() 與
與![]() 互為同分異構體
互為同分異構體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、D、E、W是中學常見的四種元素,原子序數依次增大,A的原子最外層電子數是次外層的2倍,D的氧化物屬于兩性氧化物,D、E位于同周期,A、D、E的原子最外層電子數之和為14,W是人體必需的微量元素,缺乏W會導致貧血癥狀。
(1)W在元素周期表中的位置是___。A與E組成的化合物是常用的溶劑,寫出其電子式___。
(2)下列事實能用元素周期表相應規律解釋的是(填字母序號)___。
a.D的最高價氧化物對應水化物的堿性弱于Mg(OH)2
b.E的氣態氫化物的穩定性小于HF
c.A的單質能與二氧化硅高溫下制得粗品硅單質
(3)WE3的溶液可用于刻蝕銅制的印刷電路板,反應的離子方程式為____。
(4)①工業上用電解法制備D的單質,反應的化學方程式為___。
②家用“管道通”的有效成分是燒堿和D的單質,使用時需加入一定量的水,此時發生反應的化學方程式為____。
(5)W的單質可用于處理酸性廢水中的NO3-,使其轉換為NH4+,同時生成有磁性的W的氧化物X,再進行后續處理,上述反應的離子方程式為__。上述W的氧化物X能與D的單質反應,寫出該反應的化學方程式為__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2018 年 11月,國際計量大會第 26 次會議將阿伏加德羅常數的定義修改為“1摩爾包含6.02214076×1023個基本單元,單位為 mol-1。基于這一新定義,阿伏加德羅常數的不確定度被消除了。下列說法正確的是
A.10g的1H218O含有的質子數與中子數均為5×6.02214076×1023
B.100gNaHSO4和20g KHSO3的固體混合物中陽離子數為2×6.02214076×1023
C.標準狀況下,2.24L Cl2溶于水,轉移電子數目為6.02214076×1022
D.12g金剛石中含有化學鍵的數目為4×6.02214076×1023
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在25℃時,甘氨酸在水溶液中解離情況如下: 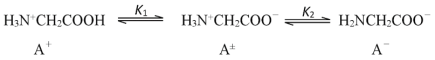 ,改變溶液pH值,三種甘氨酸相關離子的分布分數(α,平衡時某物種的濃度占各物種濃度之和的分數)變化如圖所示。當調節溶液的pH值使甘氨酸所帶的凈電荷為零,此時溶液的pH叫等電點。下列說法正確的是
,改變溶液pH值,三種甘氨酸相關離子的分布分數(α,平衡時某物種的濃度占各物種濃度之和的分數)變化如圖所示。當調節溶液的pH值使甘氨酸所帶的凈電荷為零,此時溶液的pH叫等電點。下列說法正確的是
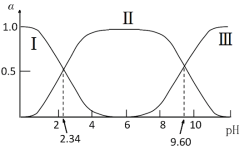
A.曲線Ⅰ、Ⅱ、Ⅲ分別代表的微粒為A-、![]() 、A+
、A+
B.K2=10-2.34,且K2對應的解離基團為—NH3+
C.在pH=9.60的溶液中加鹽酸,α(![]() )+α(A+)+α(A-)保持不變
)+α(A+)+α(A-)保持不變
D.甘氨酸的等電點pH約為6,且存在c(![]() )=c(A+)=c(A-)
)=c(A+)=c(A-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物A經李比希法和質譜法分析得知其相對分子質量為136,分子式C8H8O2。A分子中只含一個苯環且苯環上只有一個取代基,其核磁共振氫譜如圖。關于A的下列說法中,不正確的是
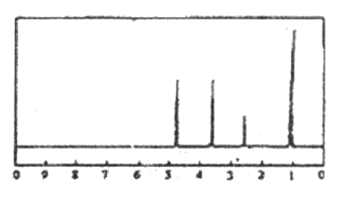
A. A分子屬于酯類化合物
B. A在一定條件下可與H2發生加成反應
C. 符合題中A分子結構特征的有機物不只有一種
D. 與A屬于同類化合物的同分異構體只有2種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列化學用語對事實的表述不正確的是
A. 硬脂酸與乙醇的酯化反應:C17H35COOH+C2H518OH![]() C17H35COOC2H5+H218O
C17H35COOC2H5+H218O
B. 常溫時,0.1 mol·L-1氨水的pH=11.1:NH3·H2O![]()
![]() +OH
+OH
C. 由Na和C1形成離子鍵的過程:![]()
D. 電解精煉銅的陰極反應:Cu2+ +2e![]() Cu
Cu
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com