
 汽車尾氣中的主要污染物是NO和CO.為減輕大氣污染,人們提出通過以下反應來處理汽車尾氣:
汽車尾氣中的主要污染物是NO和CO.為減輕大氣污染,人們提出通過以下反應來處理汽車尾氣:| 時間/s | 0 | 1 | 2 | 3 | 4 | 5 |
| C(NO)10-4 mol/L | 10.0 | 4.50 | C1 | 1.50 | 1.00 | 1.00 |
| C(CO)10-3 mol/L | 3.60 | 3.05 | C2 | 2.75 | 2.70 | 2.70 |
| 實驗 編號 | T/°C | NO初始濃 度/10-3mol•L-1 | CO初始濃 度/10-3mol•L-1 | 催化劑的比 表面積/m2•g-1 |
| ① | 350 | 1.20 | 5.80 | 124 |
| ② | 280 | 1.20 | 5.80 | 124 |
| ③ | 280 | 1.20 | 5.80 | 82 |
| 實驗組 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所 需時間/min | ||
| H2O | CO | CO | H2 | |||
| ① | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
| ② | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
| ③ | 900 | a | b | c | d | t |
分析 (1)根據蓋斯定律,由已知熱化學方程式乘以適當的系數進行加減構造目標熱化學方程式,反應熱也進行相應的計算;
(2)由表中數據可知4s時反應到達平衡,1-3s內NO濃度變化量為4.5×10-4 mol/L-1.5×10-4 mol/L=3×10-4 mol/L,該2s內平均每秒內變化量為1.5×10-4 mol/L,隨反應進行,反應速率減小,該2s中前1s內NO濃度變化量應大于1.5×10-4 mol/L,則2s時NO的濃度小于4.5×10-4 mol/L-1.5×10-4 mol/L=3×10-4 mol/L,故2s時NO的濃度應介于1.5×10-4 mol/L~3×10-4 mol/L之間;
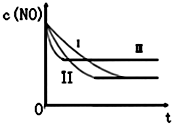
(3)由圖可知,曲線Ⅰ和曲線Ⅱ相比,平衡沒有移動,反應速率Ⅱ比Ⅰ快,故曲線Ⅱ中催化劑比比表面積大于Ⅰ,而其它條件相同;而曲線Ⅲ和曲線Ⅱ相比,反應速率變快且平衡逆向移動,該反應為放熱反應,升高溫度平衡逆向移動;
(4)①列三段表示出實驗1各物質濃度的變化情況,然后根據速率公式:v(CO2)=$\frac{△c}{△t}$;
②實驗組②和實驗組③溫度相同,平衡常數相同,根據三行式進行計算求解;
(5)①CO發生氧化反應與O2-結合生成CO32-;
②陽極上氯離子失電子,陰極上陽離子得電子.
解答 解:(1)已知:①2 NO(g)+2CO(g)?2CO2(g)+N2(g)△H=-746.5KJ/mol
②2C (s)+O2(g)?2CO(g)△H=-221.0KJ/mol
③C (s)+O2(g)?CO2(g)△H=-393.5KJ/mol
則依據蓋斯定律,③×2-②-①得到:N2(g)+O2(g)=2NO(g) 則△H=(-393.5KJ/mol)×2-(-220KJ/mol)-(-746.5KJ/mol)=+180.5KJ/mol,
故答案為:+180.5;
(2)由表中數據可知4s時反應到達平衡,1-3s內NO濃度變化量為4.5×10-4 mol/L-1.5×10-4 mol/L=3×10-4 mol/L,該2s內平均每秒內變化量為1.5×10-4 mol/L,隨反應進行,反應速率減小,該2s中前1s內NO濃度變化量應大于1.5×10-4 mol/L,則2s時NO的濃度小于4.5×10-4 mol/L-1.5×10-4 mol/L=3×10-4 mol/L,故2s時NO的濃度應介于1.5×10-4 mol/L~3×10-4 mol/L之間,選項中只有2.5×10-4 mol/L符合,
故選:D;
(3)由于②、③溫度相同,催化劑對平衡移動無影響,化學平衡不移動,達到相同的平衡狀態,但②的起始濃度較大,催化劑的比表面積較大,則反應的速率大,所以②先達到化學平衡;由于①、②濃度、催化劑的比面積大相同,而①的溫度較高,反應速率較快,先到達平衡,且平衡向逆反應移動,平衡時NO的濃度增大,
所以曲線Ⅰ對應實驗③,曲線Ⅱ對應實驗②,曲線Ⅲ對應實驗①,
故答案為:③;
(4)①H2O(g)+CO(g)?CO2(g)+H2(g)
初始 1mol/L 2mol/L 0 0
轉化 0.8mol/L 0.8mol/l 0.8mol/L 0.8mol/L
平衡0.2mol/L 1.2mol/L 0.8mol/L 0.8mol/L
v(CO2)=$\frac{△c}{△t}$=$\frac{0.8mol/L}{5min}$=0.16mol/(L•min),故答案為:0.16mol/(L•min);
②H2O(g)+CO(g)?CO2(g)+H2(g)
初始 0.5mol/L 1mol/L 0 0
轉化 0.2mol/L 0.2mol/l 0.2mol/L 0.2mol/L
平衡0.3mol/L 0.8mol/L 0.2mol/L 0.2mol/L
H2O(g)+CO(g)?CO2(g)+H2(g)
初始 1mol/L 0.5mol/L 0 0
轉化 (0.5-$\frac{c}{2}$)mol/L (0.5-$\frac{c}{2}$)mol/l $\fracp9vv5xb5{2}$mol/L $\fracp9vv5xb5{2}$mol/L
平衡(0.5+$\frac{c}{2}$)mol/L $\frac{c}{2}$mol/L $\fracp9vv5xb5{2}$mol/L $\fracp9vv5xb5{2}$mol/L
所以0.5-$\frac{c}{2}$=$\fracp9vv5xb5{2}$
則:d=1-c,由平衡常數相等可知:$\frac{\frac{1-c}{2}×\frac{1-c}{2}}{(0.5+\frac{c}{2})×\frac{c}{2}}=\frac{0.2×0.2}{0.3×0.8}$,解之得c=0.6,②中H2O(g)的轉化率為:$\frac{0.2}{0.5}×100%$=40%,實驗組③中CO的轉化率的$\frac{0.5-\frac{0.6}{2}}{0.5}$=40%,故答案為:0.6;=;
(5)①負極CO發生氧化反應與O2-結合生成CO32-,負極電極反應式為:CO+2O2--2e-=CO32-,
故答案為:CO+2O2--2e-=CO32-;
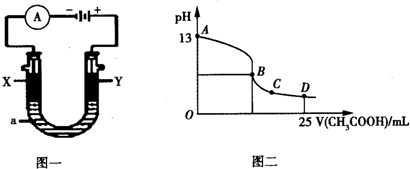
②陽極上氯離子失電子,陰極上陽離子得電子,所以電解0.1mol/L KCl溶液,其電解總反應的離子方程式為:2Cl-+2H2O$\frac{\underline{\;電解\;}}{\;}$Cl2↑+H2↑+2OH-;根據圖知,KOH溶液的pH=13,常溫下,KOH的濃度是0.1mol/L,則n(KOH)=0.1mol/L×2L=0.2mol,根據2Cl-+2H2O$\frac{\underline{\;電解\;}}{\;}$2OH-+H2↑+Cl2↑知,生成0.2mol氫氧根離子轉移電子的物質的量=$\frac{0.2mol}{2}$×2=0.2mol,燃料電池的負極反應方程式是CO+2O2--2e-=CO32-,消耗1molCO轉移電子數=2mol,因此當轉移0.2mol電子時消耗CO的物質的量為0.1mol,則CO的質量=0.1mol×28g/mol=2.8g,
故答案為:2Cl-+2H2O$\frac{\underline{\;電解\;}}{\;}$Cl2↑+H2↑+2OH-;2.8.
點評 本題考查蓋斯定律的應用,化學平衡常數的計算及應用,做題時注意影響平衡移動的因素以及平衡常數的有關計算,題目難度中等.


科目:高中化學 來源: 題型:解答題
 Na2S2O3是重要的化工原料,易溶于水,在中性或堿性環境中穩定.
Na2S2O3是重要的化工原料,易溶于水,在中性或堿性環境中穩定.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 82克O2所含有的原子數目為NA | |
| B. | 0.5molH2O含有的原子數目為1.5NA | |
| C. | 1molH2O含有的H2O分子數目為NA | |
| D. | 0.5NA個氯氣分子的物質的量是0.5mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
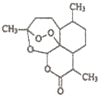 中國藥學家屠呦呦因最早發現并提純抗瘧新藥青蒿素而獲得2015年度諾貝爾生理學或醫學獎.已知青蒿素可從與青蒿同屬的黃花蒿中提取,其結構如圖所示,下列有關青蒿素說法不正確的是( )
中國藥學家屠呦呦因最早發現并提純抗瘧新藥青蒿素而獲得2015年度諾貝爾生理學或醫學獎.已知青蒿素可從與青蒿同屬的黃花蒿中提取,其結構如圖所示,下列有關青蒿素說法不正確的是( )| A. | 化學式為C15H20O5 | |
| B. | 能與NaOH溶液發生反應 | |
| C. | 與H2O2含有相似結構,具有殺菌作用 | |
| D. | 提取方法主要是低溫萃取 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 室溫下測定等濃度氨水和NaOH溶液的pH,比較氨水和NaOH堿性強弱 | |
| B. | 將氨水緩慢滴入AlCl3溶液中,研究Al(OH)3的兩性 | |
| C. | 將蘸有濃氨水和濃硫酸的玻璃棒靠近,觀察到白煙 | |
| D. | 加熱除去NH4Cl中的少量NaHC03 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③⑤ | B. | ③④⑤ | C. | ②③⑤ | D. | ②③④⑤ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com