
分析 設轉化的B為xmol/L,則
2A(g)+B (g)═3C (g)
起始濃度(mol/L) 4 2 0
轉化濃度(mol/L) 2x x 3x
平衡濃度(mol/L) 4-2x 2-x 3x
則K=$\frac{(3x)^{3}}{(4-2x)^{2}×(2-x)}$=16,
解得x=1.142mol/L,
結合轉化率=$\frac{轉化的量}{開始的量}$×100%計算.
解答 解:設轉化的B為xmol/L,則
2A(g)+B (g)═3C (g)
起始濃度(mol/L) 4 2 0
轉化濃度(mol/L) 2x x 3x
平衡濃度(mol/L) 4-2x 2-x 3x
則K=$\frac{(3x)^{3}}{(4-2x)^{2}×(2-x)}$=16,
解得x=1.142mol/L,
因此A的轉化率是$\frac{1.142mol/L×2}{4mol/L}$×100%=57.1%,
故答案為:57.1%.
點評 本題考查化學平衡的計算,為高頻考點,把握化學平衡三段法、平衡常數及轉化率的計算為解答的關鍵,側重分析與計算能力的考查,注意利用平衡濃度計算K,題目難度不大.


科目:高中化學 來源: 題型:選擇題
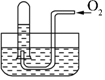 如圖所示,試管中盛裝的是紅棕色氣體(可能是混合物),當倒扣在盛有水的水槽中時,試管內水面上升,但不能充滿試管.當向試管內鼓入氧氣后,可以觀察到試管中水柱繼續上升,經過多次重復后,試管內完全被水充滿,原來試管中盛裝的可能是什么氣體( )
如圖所示,試管中盛裝的是紅棕色氣體(可能是混合物),當倒扣在盛有水的水槽中時,試管內水面上升,但不能充滿試管.當向試管內鼓入氧氣后,可以觀察到試管中水柱繼續上升,經過多次重復后,試管內完全被水充滿,原來試管中盛裝的可能是什么氣體( )| A. | 可能是N2與NO2的混合氣體 | B. | 可能是O2與NO2的混合氣體 | ||
| C. | 一定是NO與NO2的混合氣體 | D. | 只可能是NO2一種氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 原混合氣體的體積為1.2V | B. | 原混合氣體的體積為1.1V | ||
| C. | 反應達平衡時氣體B消耗掉0.05V | D. | 反應達到平衡時氣體A消耗掉0.05V |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分子間作用力越大,分子越穩定 | |
| B. | 氣態氫化物共價鍵越強,熱穩定性越高 | |
| C. | 冰融化時水分子中共價鍵發生斷裂 | |
| D. | 氫鍵是化學鍵的一種類型 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 降低N2的濃度能加快反應速率 | |
| B. | 降低體系溫度能加快反應速率 | |
| C. | 達平衡時各組分含量之比一定等于 1:3:2 | |
| D. | 達到平衡時N2的濃度不再變化 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com