
(1) ![]() 是反應性很強的正離子,是缺電子的,其電子式是:_________________。
是反應性很強的正離子,是缺電子的,其電子式是:_________________。
(2) ![]() 中4個原子是共平面的,3個鍵角相等,鍵角應是____________________。
中4個原子是共平面的,3個鍵角相等,鍵角應是____________________。
 金牌課堂練系列答案
金牌課堂練系列答案 三新快車金牌周周練系列答案
三新快車金牌周周練系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源:助學叢書(化學高二·第二冊) 題型:021
有些有機化學反應中有中間體生成,如碳正離子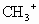 和碳自由基·
和碳自由基· 中的兩種,下列關于它們的說法中正確的是
中的兩種,下列關于它們的說法中正確的是
[ ]
A.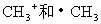 具有相同的組成,因而是相同的微粒
具有相同的組成,因而是相同的微粒
B.碳正離子和碳自由基都是共價鍵斷裂生成的
C.碳正離子帶正荷,碳自由基帶負電荷
D.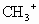 是反應性很強的正離子是缺電子的而·
是反應性很強的正離子是缺電子的而·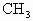 則是電中性的
則是電中性的
查看答案和解析>>
科目:高中化學 來源: 題型:021
有些有機化學反應中有中間體生成,如碳正離子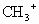 和碳自由基·
和碳自由基·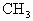 中的兩種,下列關于它們的說法中正確的是
中的兩種,下列關于它們的說法中正確的是
[ ]
A.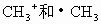 具有相同的組成,因而是相同的微粒
具有相同的組成,因而是相同的微粒
B.碳正離子和碳自由基都是共價鍵斷裂生成的
C.碳正離子帶正荷,碳自由基帶負電荷
D.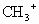 是反應性很強的正離子是缺電子的而·
是反應性很強的正離子是缺電子的而·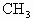 則是電中性的
則是電中性的
查看答案和解析>>
科目:高中化學 來源:2010—2011學年福建省安溪一中、養正中學高二下學期期末聯考化學試卷(理) 題型:填空題
(13分)
I、為減少溫室效應,科學家設計反應:CO2+4H2→CH4+2H2O以減小空氣中CO2。
(1)若有1mol CH4生成,則有 molσ鍵和 molπ鍵斷裂。
(2)CH4失去H—(氫負離子)形成CH+3(甲基正離子)。已知CH+3的空間結構是平面正三角形,則CH+3中碳原子的雜化方式為 。
Ⅱ、金屬原子與CO形成的配合物稱為金屬羰基配合物(如羰基鐵)。形成配合物時,每個CO提供一對電子與金屬原子形成配位鍵,且金屬原子的價電子和CO提供的電子總和等于18。
(3)金屬羰基配合物中,微粒間作用力有 (填字母代號)
a、離子鍵 b、共價鍵 c、配位鍵 d、金屬鍵
(4)羰基鐵是一種黃色油狀液體,熔點-21℃、沸點102.8℃。由此推測,固體羰基鐵更接近于 (填晶體類型)。若用Fe(CO)x表示羰基鐵的化學式,則x= 。
III.研究表明,對于中心離子為Hg2+等陽離子的配合物,若配位體給出電子能力越強:則配位體與中心離子形成的配位鍵就越強,配合物也就越穩定。
(5)預測HgCl42-與HgI42-的穩定性強弱,并從元素電負性的角度加以解釋。
答:HgCl42-比HgI42-更 (填“穩定”或“不穩定”),因為 。
查看答案和解析>>
科目:高中化學 來源:2013屆福建省漳州立人學校高二下學期期中考試化學試卷(解析版) 題型:填空題
(16分)I、為減少溫室效應,科學家設計反應:CO2+4H2==CH4+2H2O以減小空氣中CO2。
(1)若有1mol CH4生成,則有 mol σ鍵和 mol π鍵斷裂。
(2)CH4失去H—(氫負離子)形成CH+3(甲基正離子)。已知CH+3的空間結構是平面正三角形,則CH+3中碳原子的雜化方式為 。
Ⅱ、金屬原子與CO形成的配合物稱為金屬羰基配合物(如羰基鐵)。形成配合物時,每個CO提供一對電子與金屬原子形成配位鍵,且金屬原子的價電子和CO提供的電子總和等于18。
(3)金屬羰基配合物中,微粒間作用力有 (填字母代號)。
a、離子鍵 b、共價鍵 c、配位鍵 d、金屬鍵
(4)羰基鐵是一種黃色油狀液體,熔點-21℃、沸點102.8℃。由此推測,固體羰基鐵更接近于 (填晶體類型)。若用Fe(CO)x表示羰基鐵的化學式,則x= 。
III.研究表明,對于中心離子為Hg2+等陽離子的配合物,若配位體給出電子能力越強,則配位體與中心離子形成的配位鍵就越強,配合物也就越穩定。
(5)預測HgCl42-與HgI42-的穩定性強弱,并從元素電負性的角度加以解釋。
答:HgCl42-比HgI42-更 (填“穩定”或“不穩定”),因為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com