
氨氧化制硝酸的反應如下(未配平):①NH3 + O2 →NO + H2O ②NO + O2 → NO2
③NO2+H2O→HNO3+NO,如將氨全部氧化得2mol硝酸,理論上需氧氣的物質的量是( )
| A.2mol | B.3 mol | C.4 mol | D.5 mol |
 小學教材完全解讀系列答案
小學教材完全解讀系列答案科目:高中化學 來源: 題型:單選題
在100ml含等物質的量的HBr和H2SO3的溶液中通入0.025molCl2,有一半Br-變為Br2。則原溶液中HBr和H2SO3的濃度都等于( )
| A.0.16mol/L | B.0.02mol/L | C.0.20mol/L | D.0.25mol?L?1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
金屬鈰(稀土元素)性質活潑。鈰常見的化合價為+3和+4,氧化性:Ce4+>Fe3+>I2。下列說法正確的是
| A.鈰溶于氫碘酸的化學方程式可表示為:Ce + 4HI = CeI4 + 2H2↑ |
| B.用Ce(SO4)2溶液滴定硫酸亞鐵溶液,其離子方程式為:Ce4+ + Fe2+=Ce3+ + Fe3+ |
| C.在一定條件下,電解熔融狀態的CeO2制Ce,在陽極獲得鈰 |
D.四種鈰的核素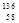 Ce、 Ce、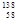 Ce、 Ce、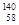 Ce、 Ce、 Ce,它們互稱為同素異形體 Ce,它們互稱為同素異形體 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
已知R有多種化合價,其最高正價為+7價。在一定條件下,RO3-與R-可發生反應:RO3-+5R-+6H+=3R2+3H2O,下列關于R元素的敘述中,正確的是( )
| A.元素R位于周期表中第VA族 |
| B.RO3-中的R只能被還原 |
| C.R-離子的最外層電子數為8 |
| D.若1 mol RO3-參與該反應,則轉移的電子的物質的量為5mol |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
ClO2氣體是一種常用的消毒劑,我國從2 000年起逐步用ClO2代替氯氣對飲用水進行消毒。
(1)消毒水時,ClO2還可將水中的Fe2+、Mn2+等轉化成Fe(OH)3和MnO2等難溶物除去,在這個過程中,Fe2+、Mn2+的化合價升高,說明ClO2具有______性。
(2)工業上可以通過下列方法制取ClO2,請完成該化學反應方程式:
2KClO3+SO2===2ClO2+__________。
(3)自來水廠用ClO2處理后的水中,要求ClO2的濃度在0.1~0.8 mg·L-1之間。碘量法可以檢測水中ClO2的濃度,步驟如下:
Ⅰ.取一定體積的水樣,加入一定量的碘化鉀,再用氫氧化鈉溶液調至中性,并加入淀粉溶液,溶液變藍。
Ⅱ.加入一定量的Na2S2O3溶液。(已知:2S2O +I2===S4O
+I2===S4O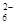 +2I-)
+2I-)
Ⅲ.加硫酸調節水樣pH至1~3。
操作時,不同pH環境中粒子種類如下圖所示: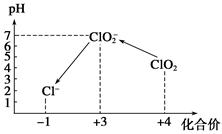
請回答:
①操作Ⅰ中反應的離子方程式是______________________________。
②確定操作Ⅱ完全反應的現象是______________________________。
③在操作Ⅲ過程中,溶液又呈藍色,反應的離子方程式是__________________。
④若水樣的體積為1.0 L,在操作Ⅱ時消耗了1.0×10-3 mol·L-1的Na2S2O3溶液10 mL,則水樣中ClO2的濃度是________mg·L-1。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(13分)某研究性學習小組利用廢舊鉛蓄電池陰、陽極填充物------鉛膏(含PbO、PbO2、PbSO4)制備電絕緣材料三鹽基硫酸鉛(3PbO?PbSO4?H2O),進行資源回收研究,設計實驗流程如下: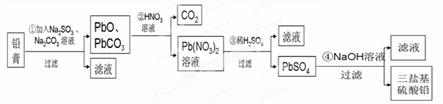
(1)步驟①鉛膏中PbSO4與Na2CO3溶液反應轉化為PbCO3,說明溶解度:PbSO4 (填“>”或“<”)PbCO3。
(2)步驟①中PbO2轉化為PbCO3的離子方程式是(請配平此離子方程式):
(3)將步驟①和④的濾液合并,加入 PH=7,再經過 、冷卻結晶、
、洗滌、干燥,可獲得Na2SO4?10H2O晶體。
(4)若鉛膏的質量為78g,步驟①中PbO2和PbSO4全部轉化為PbCO3,且PbO未發生反應;步驟②中共收集到5.6LCO2(標準狀態),步驟③中獲得90.9 g PbSO4,則鉛膏中PbO的質量分數為 (假設流程中原料無損失)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
利用I2O5可消除CO污染或定量測定CO,反應為:5CO(g)+I2O5(s) 5CO2(g)+I2(s);ΔH 1
5CO2(g)+I2(s);ΔH 1
(1)已知:2CO(g)+O2(g) 2CO2(g);ΔH 2
2CO2(g);ΔH 2
2I2(s)+5O2(g) 2I2O5(s);ΔH 3
2I2O5(s);ΔH 3
則ΔH 1= (用含ΔH 2和ΔH 3的代數式表示)。
(2)不同溫度下,向裝有足量I2O5固體的2 L恒容密閉容器中通入2molCO,測得CO2的體積分數φ(CO2)隨時間t變化曲線如圖。請回答:
①從反應開始至a點時的反應速率為v(CO)= ,b點時化學平衡常數Kb= 。
②d點時,溫度不變,若將容器體積壓縮至原來的一半,請在圖中補充畫出CO2體積分數的變化曲線。
③下列說法正確的是 。(填字母序號)
| A.容器內氣體密度不變,表明反應達到平衡狀態 |
| B.兩種溫度下,c點時體系中混合氣體的平均相對分子質量相等 |
| C.增加I2O5的投料量有利于提高CO的轉化率 |
| D.b點和d點的化學平衡常數:Kb<Kd |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com