
甲、乙兩種非金屬:①甲的最高價氧化物對應的水化物酸性比乙的最高價氧化物對應的水化物酸性強;②甲比乙更容易與氫氣化合;③甲單質能與乙陰離子發生氧化還原反應;④與金屬反應時,甲原子得電子數目比乙的多;⑤甲的單質熔沸點比乙的低。能說明甲比乙的非金屬性強的是( )
A. ①②③④ B. ①②③④⑤ C. ①②③ D. ②③④⑤
 優質課堂快樂成長系列答案
優質課堂快樂成長系列答案科目:高中化學 來源:2016-2017學年遼寧省大連市高二上9月月考化學試卷(解析版) 題型:推斷題
短周期的五種主族元素A、B、C、D、E原子序數依次變小。A的單質在常溫下為氣態,屬于同一主族,C為自然界含量最多的金屬元素,D的最外層電子數為次外層的2倍,E為周期表中原子半徑最小的元素。
(1)A、B的元素名稱分別為___________、___________。
(2)A、D氫化物中穩定性強的氫化物是__________________
(3)A、C的最高價氧化物的水化物反應的離子方程式是__________________。
(4) 用化學反應方程式及必要的文字說明B、D非金屬性的強弱________________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河南省許昌市五校高二上學期第一次聯考化學試卷(解析版) 題型:選擇題
有A、B、C、D、E五種短周期元素,其中A、B、C、D同周期, C、E同主族; A+ 與E2-具有相同的電子層結構;離子半徑:C2->D-;B的單質晶體熔點、硬度大,是一種重要的半導體材料。下列說法中,正確的是( )
A. 由于D、C、E元素的氫化物相對分子質量依次減小,所以其沸點依次降低
B. 元素D和E的某些單質不可以作為水處理中的消毒劑
C. 元素B的單質只能與氫氧化鈉溶液反應而不能與任何酸反應
D. A、E兩種元素能形成A2E和A2E2型化合物
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省高二上學期9月調研化學試卷(解析版) 題型:選擇題
能說明某烴分子里含有碳碳不飽和鍵的敘述是( )
A.分子組成中含碳氫原子數之比為1:2
B.完全燃燒生產等物質的量的CO2和H2O
C.能與溴加 成反應而使溴水褪色,還能使KMnO4酸性溶液褪色
成反應而使溴水褪色,還能使KMnO4酸性溶液褪色
D. 空氣中燃燒能產生黑煙
空氣中燃燒能產生黑煙
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省高二上學期9月調研化學試卷(解析版) 題型:選擇題
天然氣根據成分不同分為貧氣和富氣,貧氣中甲烷的含量較多,富氣中乙烷、丙烷、丁烷的含量相對高一些。若要將它們液化,下列說法正確的是( )
A.貧氣易液化 B.富氣易液化
C.二者液化條件相同 D.減壓降溫均有利于兩者液化
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省高二上期初考試化學卷(解析版) 題型:填空題
甲醇(CH3OH)是一種重要的化工原料,廣泛應用于化工生產,也可以直接用做燃料。
已知:CH3OH(1)+ O2(g) =CO(g) + 2H2O(g) ;△Ha = -443.64 kJ·mol-1
2CO (g) + O2(g) = 2CO2(g) ;△Hb =-566.0 kJ·mol-1
(1)試寫出CH3OH(1)在氧氣中完全燃燒生成CO2和H2O(g)的熱化學方程式: 。
(2) CH3OH和H2的燃燒熱分別為△H=-725.5kJ/mol、△H=-285.8kJ/mol,寫出工業上以CO2和H2為原料合成CH3OH的熱化學方程式____________________。
(3)科研人員新近開發出一種由甲醇和氧氣以強堿做電解質溶液的新型手機電池,可使手機連續使用一個月才充一次電,據此回答下列問題: 甲醇在 極反應;電極反應式為 。
(4)利用電池可實現電能向化學能轉化。某同學設計了一種電解法制取Fe(OH)2的實驗裝置(如下圖所示),通電后,溶液中產生大量的白色沉淀,且較長時間不變色。下列說法中正確的是 (填序號)

A.電源中的a一定為正極,b一定為負極 B.可以用NaCl溶液作為電解液
C.A、B兩端都必須用鐵作電極 D.陰極發生的反應是:2H+ + 2e-→H2↑
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省高二上期初考試化學卷(解析版) 題型:選擇題
某有機物的結構簡式如圖,下列敘述正確的是:( )
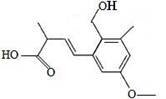
A.該有機物的分子式為C14H 20O4
B.該有機物能發生取代、加成和聚合反應
C.1 mol該有機物最多能與3 mol NaOH反應
D.該有機物分子中所有碳原子一定共平面
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江省高二上開學測化學卷(解析版) 題型:填空題
在某個容積為2 L的密閉容器內,在T℃時按下圖1所示發生反應:
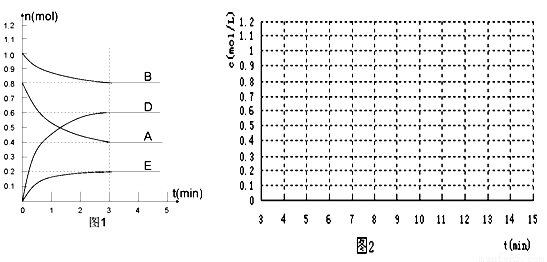
mA(g)+nB(g) pD(g)+qE(s) ?H<0(m、n、p、q為最簡比例的整數)。
pD(g)+qE(s) ?H<0(m、n、p、q為最簡比例的整數)。
(1)根據圖1所示,反應開始至達到平衡時,用D表示該反應速率為____________ mol/(L·min);方程式中m:n:p:q =________________
(2)該反應的化學平衡常數K為_________________(保留至一位小數);
(3)下列措施能增大B的轉化率的是 ( )
A. 升高溫度 B.保持體積不變通入1molB
升高溫度 B.保持體積不變通入1molB
C.保持體積不變移出部分物質D(g) D.將容器的容積增大為原來的2倍
E. 保持體積不變通入1mol A
(4)能判斷該反應已經達到化學平衡狀態的是( )
A.恒容恒溫時容器中氣體壓強保持不變
B.混合氣體中D濃度不變
C.v(A)正 = v(A)逆
D.恒容時容器中氣體密度不變
(5)反應達到平衡后,第7 min時,改變條件,在第9min達到新的平衡, 在圖2上作出第7 min至第
在圖2上作出第7 min至第 15 min(作在答題紙上):下列情況下,D濃度變化圖像
15 min(作在答題紙上):下列情況下,D濃度變化圖像
①若降低溫度且平衡時D物質的量變化了0.4 mol (用虛線)
②若將容器的容積壓縮為原來一半(用實線)
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省高二上9.4周考化學卷(解析版) 題型:選擇題
下列實驗裝置,試劑選用或操作正確的是( )
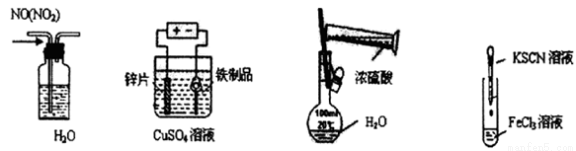
A. 除去NO中的NO2 B. 鐵制品表面鍍鋅 C. 稀釋濃硫酸 D. 鑒定Fe3+
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com