
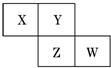
 X、Y、Z、W均為短周期元素,它們在元素周期表中的相對位置如圖所示.若Z原子的最外層電子數是第一層電子數的3倍,下列說法中正確的是( )
X、Y、Z、W均為短周期元素,它們在元素周期表中的相對位置如圖所示.若Z原子的最外層電子數是第一層電子數的3倍,下列說法中正確的是( )| A. | X的最常見氣態氫化物的水溶液顯酸性 | |
| B. | 最高價氧化物對應水化物的酸性W比Z強 | |
| C. | Z的單質與氫氣反應比Y單質與氫氣反應劇烈 | |
| D. | X的原子半徑小于Y |
分析 X、Y、Z、W均為短周期元素,Z原子的最外層電子數是第一層電子數的3倍,則Z的第一層電子數為2,最外層電子數為6,所以Z應為S,結合位置可知,Y為O,X為N,W為Cl,并利用元素及其單質、化合物的性質來解答.
解答 解:X、Y、Z、W均為短周期元素,Z原子的最外層電子數是第一層電子數的3倍,則Z的第一層電子數為2,最外層電子數為6,所以Z應為S,結合位置可知,Y為O,X為N,W為Cl,
A.X的最常見氣態氫化物為氨氣,其水溶液顯堿性,故A錯誤;
B.非金屬性Cl>S,所以最高價氧化物對應水化物的酸性W比Z強,故B正確;
C.非金屬性O>S,所以Y的單質與氫氣反應較Z劇烈,故C錯誤;
D.同周期從左向右原子半徑在減小,則X的原子半徑大于Y,故D錯誤;
故選B.
點評 本題考查位置、結構、性質的應用,Z為解答本題的突破口,元素的推斷及熟悉元素及其化合物的性質是解答本題的關鍵,題目難度不大.


 精英口算卡系列答案
精英口算卡系列答案 應用題點撥系列答案
應用題點撥系列答案科目:高中化學 來源: 題型:解答題
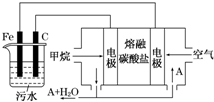 電浮選凝聚法是工業上采用的一種污水處理方法:保持污水的pH在5.0~6.0之間,通過電解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉積下來,具有凈化水的作用.陰極產生的氣泡把污水中懸浮物帶到水面形成浮渣層,刮去(或撇掉)浮渣層,即起到了浮選凈化的作用.某科研小組用電浮選凝聚法處理污水,設計裝置示意圖,如圖所示.
電浮選凝聚法是工業上采用的一種污水處理方法:保持污水的pH在5.0~6.0之間,通過電解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉積下來,具有凈化水的作用.陰極產生的氣泡把污水中懸浮物帶到水面形成浮渣層,刮去(或撇掉)浮渣層,即起到了浮選凈化的作用.某科研小組用電浮選凝聚法處理污水,設計裝置示意圖,如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=1的溶液中:Al3+、Mg2+、Cl-、SO42- | |
| B. | 使pH試紙顯藍色的溶液中:Cu2+、Fe2+、NO3-、SO42- | |
| C. | 滴入甲基橙指示劑呈紅色的溶液中:K+、NH4+、CO32-、NO3- | |
| D. | 水電離出的c(H+)=1×10-13mol•L-1的溶液中:K+、NH4+、HCO3-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | AgNO3溶液中加入過量的氨水:Ag++NH3•H2O=AgOH↓+NH4+ | |
| B. | 銨明礬[NH4Al(SO4)2•12H2O]溶液中加入過量Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O | |
| C. | H2O2溶液中滴加酸性KMnO4溶液:2 MnO4-+5 H2O2+6H+=2Mn2++5O2↑+8H2O | |
| D. | 尼泊金酸(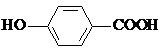 )與碳酸氫鈉溶液反應: )與碳酸氫鈉溶液反應: |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③④ | B. | ②③⑤ | C. | ③④⑤ | D. | ④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
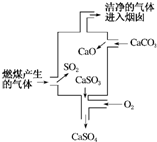
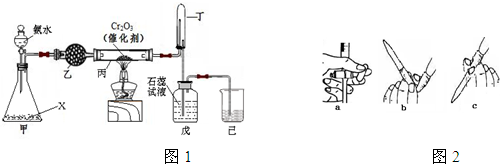
| A. | 使用此裝置處理過的廢氣就不會對大氣造成污染了 | |
| B. | 裝置內發生的反應有化合、分解、置換和氧化還原反應 | |
| C. | 整個過程的反應可表示為2SO2+2CaCO3+O2═2CaSO4+2CO2 | |
| D. | 可用澄清的石灰水檢驗經過處理的廢氣是否達標 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
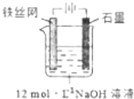 高鐵酸鉀(K2FeO4)是一種高效多功能水處理劑,具有極強的氧化性.
高鐵酸鉀(K2FeO4)是一種高效多功能水處理劑,具有極強的氧化性.| 干法 | Fe2O3、KNO3、KOH混合加熱共熔生成紫紅色高鐵酸鹽和KNO2等產物 |
| 濕法 | 強堿性介質中,Fe(NO3)3與NaClO反應生成紫紅色高鐵酸鹽溶液 |
| 電解法 | 制備中間產物Na2FeO4,再與KOH溶液反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原溶液中投入鐵粉物質的量是0.25 mol | |
| B. | 原溶液中HNO3的濃度是2.0 mol•L-1 | |
| C. | 反應后的溶液中還可溶解9.6 g銅 | |
| D. | 反應后的溶液中c(Fe2+):c(Fe3+)=1:2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com