
(8分)如圖所示,一密閉容器被無摩擦、可滑動的兩隔板a、b分成甲、乙兩室;標準狀況下,在乙室中充入0.6mol HCl,甲室中充入NH3、H2的混合氣體,靜止時活塞位置如下圖。已知甲、乙兩室中氣體的質量之差為10.9g。
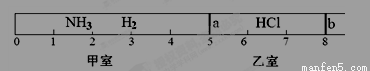
(1)甲室中氣體的物質的量為 。
(2)甲室中氣體的質量為 。
(3)甲室中NH3,H2的物質的量之比為 。
(4)將隔板a去掉,發生下列反應:HCl(g)+NH3(g)=NH4Cl(s),當HCl與NH3充分反應后,活塞b將位于刻度“ ”處(填數字)。
科目:高中化學 來源:2016屆河南省高三第二次月考化學試卷(解析版) 題型:選擇題
在一種酸性溶液中可能存在Fe3+、NO3-、Cl-、I-中的一種或幾種離子,向溶液中加入溴水,溴單質被還原,由此可推斷溶液中
A.一定含有I-,不能含有Cl- B.可能含有Cl-、NO3-和I-
C.可能含有NO3- D.不含有Fe3+
查看答案和解析>>
科目:高中化學 來源:2016屆河北省冀州市高三復習班上第一次月考化學試卷A(解析版) 題型:選擇題
向18.4 g鐵和銅組成的合金中加入過量的硝酸溶液,合金完全溶解,同時生成NO2、NO混合氣體,再向所得溶液中加入足量的NaOH溶液,生成30.3 g沉淀。另取等質量的合金,使其與一定量的Cl2恰好完全反應,則Cl2 的體積在標準狀況下為
A.7.84L B.6.72L C.4.48L D.無法計算
查看答案和解析>>
科目:高中化學 來源:2016屆安徽省合肥市高三上第二次段考化學試卷(解析版) 題型:填空題
(15分)鐵是目前人類使用量最大的金屬,它能形成多種化合物。
(1)取5.6 g的生鐵與足量的稀硫酸混合反應,無論怎樣進行實驗,最終收集了的氣體體積均小于2.24 L(標準狀況),最主要的原因是__________,所得溶液在長時間放置過程中會慢慢出現淺黃色,試用離子方程式解釋這一變化的原因____________。
(2)ZnFe2Ox是一種新型納米材料,可將工業廢氣中的某些元素轉化為游離態,制取納米ZnFe2Ox 和用于除去廢氣的轉化關系如圖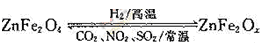 。若上述轉化反應中消耗的
。若上述轉化反應中消耗的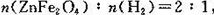 ,x的值為_________________。請寫出 ZnFe2Ox與NO2 反應的化學方程式______________(x用前一問求出的具體值)。
,x的值為_________________。請寫出 ZnFe2Ox與NO2 反應的化學方程式______________(x用前一問求出的具體值)。
(3)LiFePO4(難溶干水)材料被視為最有前途的鋰離子電池材料之一。
①以 FePO4(難溶于水)、Li2CO3 、單質碳為原料在高溫下制備LiFePO4 ,,該反應還生成一種可燃性氣體,則反應方程式為____________.
②磷酸鐵鋰動力電池有幾種類型,其中一種(中間是鋰離子聚合物的隔膜,它把正極與負樁隔開)工作原理為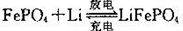 。則放電時正極上的電極反應式為___________.
。則放電時正極上的電極反應式為___________.
(4)已知25℃時,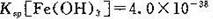 ,此溫度下若在實驗室中配制5 mol/L 100 mL FeCl3溶液,為使配制過程中不出現渾濁現象,則至少需要加人2 mol/L的鹽酸__________ml(忽略加入鹽酸體積)。
,此溫度下若在實驗室中配制5 mol/L 100 mL FeCl3溶液,為使配制過程中不出現渾濁現象,則至少需要加人2 mol/L的鹽酸__________ml(忽略加入鹽酸體積)。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年西藏日喀則一中高二10月月考化學試卷(解析版) 題型:選擇題
X、Y、Z、R和W代表原子序數依次增大的5種短周期元素,X元素原子最外層電子數比次外層電子數多2,R與Y同主族,W元素族序數等于周期數的2倍。已知常溫下:W氫化物(氣態)+Z單質(氣態)=Z氫化物(液態)+W單質(固態)。下列說法正確的是
A.Y、W元素氧化物對應的水化物一定是強酸
B.R元素位于第二周期第VA族
C.穩定性:Z氫化物>W氫化物
D.原子半徑從小到大:Z<X<Y<R
查看答案和解析>>
科目:高中化學 來源:2016屆河南省洛陽市高三上學期周練化學試卷(解析版) 題型:實驗題
已知:過氧化鈣與CO2反應有氣體生成,而將SO2通入過氧化鈣粉末中也有氣體生成。有人提出:CO2、SO2與過氧化鈣的反應原理相同,但也有人提出SO2具有較強的還原性,CO2無強還原性,反應原理不相同。據此設計如下實驗操作進行判斷。
實驗一:通過測量氣體的體積判斷發生的化學反應,實驗裝置如下
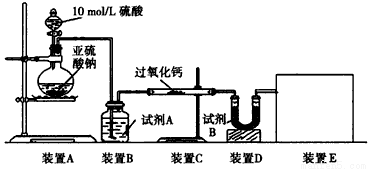
(1)試劑A可以選用_______,試劑B的作用是_______。
(2)裝置E用于測定氧氣的體積 ,請在方框中畫出裝置圖。
,請在方框中畫出裝置圖。
(3)實驗測得裝置C中過氧化鈣質量增加了m1g,裝置D質量增加了m2g,裝置E中收集到的氣體為VL(已換算成標準狀況下),用上述有關測量數據判斷,SO2未被氧化、部分被氧化、完全被氧化的V-m1 關系式。
未被氧化:__________,部分被氧化:__________, 完全被氧化:__________。
若SO2完全被氧化,寫出反應的化學方程式:__________________。
實驗二:向一定量的過氧化鈉固體中通入足量SO2,取反應后的固體進行實驗探究,以證明過氧化物與SO2反應的特點。
(4)提出假設:
假設1:反應后固體中只有__________,證明SO2未被氧化;
假設2:反應后固體中只有__________,證明SO2完全被氧化;
假設3:______________。
實驗探究:
(5)設計實驗,證明假設3是正確的,簡要回答實驗過程、現象和結論:_______。
實驗評價:
(6)實驗過程中SO2的通入量直接影響探究實驗結果的科學性,請簡要說明原因: 。
查看答案和解析>>
科目:高中化學 來源:2016屆河北省衡水市高三復習班上月考化學試卷(解析版) 題型:選擇題
短周期中的A、B、C、D、E五種元素,原子序數依次增大,A和D,C和E分別同主族,A為非金屬元素,且A與B的原子序數之和等于C的原子序數,C2—與D+的核外電子數相等。則下列說法正確的是
A.B與A只能組成BA3化合物
B.第三周期中,D原子的原子半徑最大
C.A、B、C三元素不可能形成離子化合物
D.E的氧化物對應水化物一定有強的氧化性
查看答案和解析>>
科目:高中化學 來源:2014-2015學年海南華僑中學高三第一次模擬考試化學試卷(解析版) 題型:選擇題
化學反應A2+B2=2AB的能量變化如圖所示,則下列說法正確的是
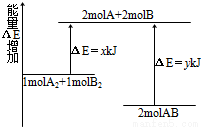
A.該反應是吸熱反應
B.斷裂2molA-B鍵需要吸收ykJ能量
C .2molAB的總能量高于1molA2和1molB2的總能量
D.斷裂1molA-A鍵和1molB-B鍵可放出xkJ能量
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com