
| △C |
| △t |
| n |
| V |
| △C |
| △t |
| ||
| 2mol×0.06L |
| 22.4L |
| 0.0054mol |
| 0.05L |
| △C |
| △t |


科目:高中化學 來源: 題型:
 某興趣小組進行“活潑金屬與酸反應”的實驗,將5.4g的鋁片投入500mL 0.5mol?L-1的硫酸溶液中,右圖為反應產生氫氣速率與反應時間的關系圖.
某興趣小組進行“活潑金屬與酸反應”的實驗,將5.4g的鋁片投入500mL 0.5mol?L-1的硫酸溶液中,右圖為反應產生氫氣速率與反應時間的關系圖.查看答案和解析>>
科目:高中化學 來源: 題型:
 NO3-+
NO3-+ ═
═ Fe2++
Fe2++ NH4++
NH4++
查看答案和解析>>
科目:高中化學 來源: 題型:
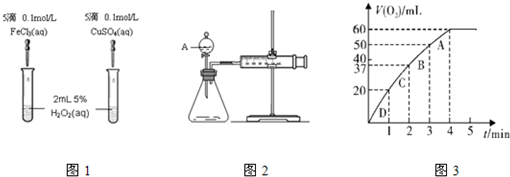
 某同學設計實驗驗證非金屬元素的非金屬性越強,對應的最高價含氧酸的酸性就越強.他設計了如圖裝置以驗證碳、氮、硅元素的非金屬性強弱.該同學設計的實驗可直接證明三種酸的酸性強弱,已知A是強酸,常溫下可與銅反應;B是塊狀固體;打開分液漏斗的活塞后,C中可觀察到白色沉淀生成.
某同學設計實驗驗證非金屬元素的非金屬性越強,對應的最高價含氧酸的酸性就越強.他設計了如圖裝置以驗證碳、氮、硅元素的非金屬性強弱.該同學設計的實驗可直接證明三種酸的酸性強弱,已知A是強酸,常溫下可與銅反應;B是塊狀固體;打開分液漏斗的活塞后,C中可觀察到白色沉淀生成.查看答案和解析>>
科目:高中化學 來源: 題型:
| 1 |
| 2 |
| A、40% | B、50% |
| C、70% | D、80% |
查看答案和解析>>
科目:高中化學 來源: 題型:
 溴乙烷在不同溶劑中與NaOH可發生不同類型的反應,生成不同的反應產物.
溴乙烷在不同溶劑中與NaOH可發生不同類型的反應,生成不同的反應產物.查看答案和解析>>
科目:高中化學 來源: 題型:
| A、C2H4 |
| B、C4H8 |
| C、C4H10 |
| D、C5H10 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、等質量的鋁分別與足量氫氧化鈉溶液和稀硝酸反應,放出的氫氣一樣多 |
| B、將SO2通入過量Ba(NO3)2溶液可生成BaSO4沉淀 |
| C、自來水廠常用明礬對水進行殺菌、消毒 |
| D、將稀硫酸滴加到Fe(NO3)2溶液中無明顯現象 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、某學生用pH試紙測新制氯水的pH值,先變紅后褪色,是因為Cl2有強氧化性 |
| B、向氯水中加入碳酸氫鈉粉末,有氣泡產生,說明氯水中含有H+ |
| C、配制一定物質的量濃度的溶液發現濃度偏低,可能由于配制溶液所用的容量瓶事先未干燥 |
| D、將銅片放入濃硫酸中,無明顯實驗現象,說明銅在冷的濃硫酸中發生鈍化 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com