
| A. | ①②③ | B. | ①③④ | C. | ③④⑤ | D. | ①③⑤ |
分析 ①淀粉水解生成葡萄糖,油脂水解生成甘油和高級脂肪酸或鹽,蛋白質水解生成氨基酸;
②汽油中加入適量乙醇,為混合物;
③乙酸與碳酸鈉反應后,與乙酸乙酯分層;
④分餾與物質沸點有關;
⑤淀粉遇碘變藍,葡萄糖具有還原性,能被弱氧化劑氧化.
解答 解:①淀粉水解生成葡萄糖,油脂水解生成甘油和高級脂肪酸或鹽,蛋白質水解生成氨基酸,則均可在一定條件下水解,故正確;
②汽油中加入適量乙醇,為混合物,不是化合物,故錯誤;
③乙酸與碳酸鈉反應后,與乙酸乙酯分層,然后分液可分離,故正確;
④分餾與物質沸點有關,為物理變化,而煤的氣化是發生了化學變化,故錯誤;
⑤淀粉遇碘變藍,葡萄糖具有還原性,能被弱氧化劑氧化,則淀粉遇碘酒變藍色,在加熱條件下葡萄糖能與新制Cu(OH)2懸濁液發生反應,故正確;
故選D.
點評 本題考查有機物的結構與性質,為高頻考點,把握官能團與性質的關系、有機反應、混合物分離提純等為解答的關鍵,側重分析與應用能力的考查,題目難度不大.


 課時訓練江蘇人民出版社系列答案
課時訓練江蘇人民出版社系列答案科目:高中化學 來源: 題型:解答題
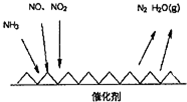
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
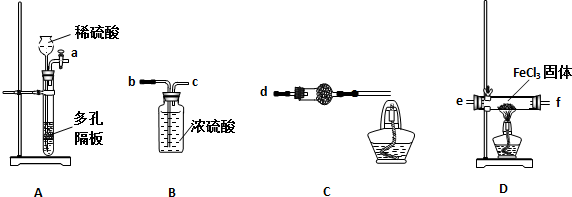
| 滴定次數 | 標準溶液的體積 | |
| 滴定前刻度/mL | 滴定后刻度/mL | |
| 1 | 1.04 | 25.03 |
| 2 | 1.98 | 25.99 |
| 3 | 3.20 | 25.24 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
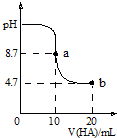 室溫下向10mL0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的變化曲線如圖所示.下列說法正確的是( )
室溫下向10mL0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的變化曲線如圖所示.下列說法正確的是( )| A. | a點所示溶液中c(Na+)>c(A-)>c(H+)>c(HA) | |
| B. | pH=7時,c(Na+)=0.05 mol•L-1 | |
| C. | a、b兩點溶液中水電離出c(H+)濃度的比值為104 | |
| D. | b點所示溶液中c(A-)<c(HA) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4 L水中含有的水分子數為NA | |
| B. | 4.0 g NaOH固體溶于100 mL水中,得到1 mol/L的 NaOH溶液 | |
| C. | 常溫、常壓下,22 g CO2中含有的氧原子數為NA | |
| D. | 0.5 mol/L Na2SO4溶液中,含有的離子總數為1.5NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
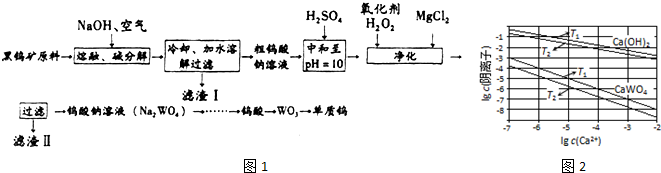
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com