
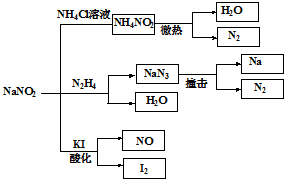
 亞硝酸鈉(NaNO2)是一種工業用鹽,廣泛用于物質合成、金屬表面處理等,它的一些性質見如圖.下列說法不正確的是( )
亞硝酸鈉(NaNO2)是一種工業用鹽,廣泛用于物質合成、金屬表面處理等,它的一些性質見如圖.下列說法不正確的是( )| A、NH4NO2的熱穩定性大于NaNO2 |
| B、NaN3分解,每產生1molN2轉移6mole- |
| C、NaN3可用氨基鈉(NaNH2)和N2O在液氨中低溫制備,N2O與N3-互為等電子體 |
| D、可用淀粉碘化鉀試紙和食醋鑒別NaCl與NaNO2 |
| 1 |
| 3 |
| 2 |
| 3 |
| 1 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |


 口算題天天練系列答案
口算題天天練系列答案科目:高中化學 來源: 題型:
 (I)如圖是某學校林老師制備NH3并進行性質實驗時的改進裝置.按圖1把儀器安裝好,稱取2g固體氯化銨裝入試管底部,再稱取2g氫氧化鈉覆蓋在氯化銨上方;立即用帶有滴管的塞子塞緊(滴管預先吸入約2mL濃氨水);燒杯內盛滴有酚酞試液的水:把濃氨水滴入試管里,可立即觀察到試管內發生劇烈反應,有大量氣泡.
(I)如圖是某學校林老師制備NH3并進行性質實驗時的改進裝置.按圖1把儀器安裝好,稱取2g固體氯化銨裝入試管底部,再稱取2g氫氧化鈉覆蓋在氯化銨上方;立即用帶有滴管的塞子塞緊(滴管預先吸入約2mL濃氨水);燒杯內盛滴有酚酞試液的水:把濃氨水滴入試管里,可立即觀察到試管內發生劇烈反應,有大量氣泡.查看答案和解析>>
科目:高中化學 來源: 題型:
A、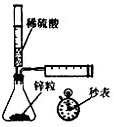 測定一定時間內生成H2的反應速率 |
B、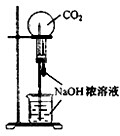 用CO2做噴泉實驗 |
C、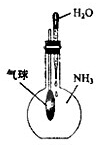 驗證NH3易溶于水 |
D、 比較Na2CO3與NaHCO3的熱穩定性 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、Zn、Ag |
| B、Cu、Fe |
| C、Al、Fe |
| D、Mg、Al |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、1:2 |
| B、8:1 |
| C、35.5:108 |
| D、108:35.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 化學式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2ClO3 |
| Ksp或Ka | Ksp=1.8×10-10 | Ksp=2.0×10-12 | Ka=1.8×105 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=1.8×10-11 |
| A、相同濃度CH3COONa和NaClO的混合液中,各離子濃度的大小關系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) |
| B、碳酸鈉溶液中滴加少量氯水的離子方程式為CO2-3+Cl2+H2O=HCO-3+Cl-+HClO |
| C、向0.1mol?L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此時溶液pH=5 |
| D、向濃度均為1×10-3mol?L-1的KCl和K2CrO4混合液中滴加1×10-3mol?L-1的AgNO3溶液,CrO2-4先形成沉淀 |
查看答案和解析>>
科目:高中化學 來源: 題型:
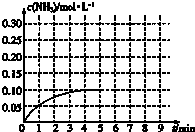 在一容積為2L的密閉容器內加入0.2mol的N2和0.6mol的H2,在一定條件下發生如下反應:N2(g)+3H2(g)?2NH3(g)△H<0,反應中NH3的物質的量濃度的變化情況如圖:
在一容積為2L的密閉容器內加入0.2mol的N2和0.6mol的H2,在一定條件下發生如下反應:N2(g)+3H2(g)?2NH3(g)△H<0,反應中NH3的物質的量濃度的變化情況如圖:查看答案和解析>>
科目:高中化學 來源: 題型:
| A、AlCl3溶液與稀氨水 |
| B、FeBr2溶液與Cl2 |
| C、CO2與Na2SiO3溶液 |
| D、澄清石灰水與Ca(HCO3)2溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、兩項 | B、三項 | C、四項 | D、五項 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com