
| 名稱 | 氧化鐵 | 碳酸鈉 | 碳酸氫鈉 |
| 俗名 | 鐵紅 | 小蘇打 | |
| 化學式 | Na2CO3 | NaHCO3 |
分析 (1)鈉是活潑金屬容易和氧氣、水、二氧化碳等物質發生反應,自然界中以化合態存在;
(2)Fe元素的化合價降低,則維生素C中某元素的化合價升高;
(3)依據物質的名稱、俗稱、化學式和物質的分類解答,鐵紅是氧化鐵,碳酸鈉俗稱為純堿;
(4)碳酸鈉是鹽易溶于水,在水溶液中完全電離;硫酸銅和鐵反應生成銅和硫酸亞鐵.
解答 解:(1)鈉是活潑金屬容易和空氣中的氧氣、水、二氧化碳等物質發生反應,那在自然界中以化合態存在,
故答案為:水,化合;
(2)Fe元素的化合價降低,則維生素C中某元素的化合價升高,說明維生素C具有還原性,故答案為:還原性;
(3)鐵紅是氧化鐵,化學式為:Fe2O3,碳酸鈉俗稱為純堿或蘇打,
故答案為:
| 名稱 | |||
| 俗名 | 純堿或蘇打 | ||
| 化學式 | Fe2O3 |
點評 本題考查了物質分類、物質性質、物質俗稱、物質電離方程式和化學方程式書寫,掌握基礎是解題關鍵,題目較簡單.


 學練快車道快樂假期暑假作業新疆人民出版社系列答案
學練快車道快樂假期暑假作業新疆人民出版社系列答案 浙大優學小學年級銜接導與練浙江大學出版社系列答案
浙大優學小學年級銜接導與練浙江大學出版社系列答案 小學暑假作業東南大學出版社系列答案
小學暑假作業東南大學出版社系列答案 津橋教育暑假拔高銜接廣東人民出版社系列答案
津橋教育暑假拔高銜接廣東人民出版社系列答案科目:高中化學 來源: 題型:解答題
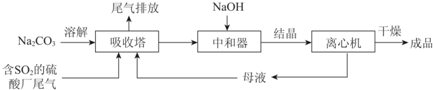
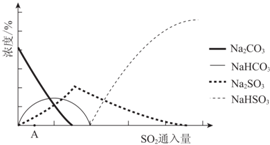
| 資料顯示: Ⅰ.Na2SO3在33℃時溶解度最大,將其飽和溶液加熱至33℃以上時,由于溶解度降低會析出無水Na2SO3,冷卻至33℃以下時析出Na2SO3•7H2O; Ⅱ.無水Na2SO3在空氣中不易被氧化,Na2SO3•7H2O在空氣中易被氧化. |
 2Na+ (aq)+SO32- (aq),NaOH過量使c(Na+)增大,上述平衡逆向移動.
2Na+ (aq)+SO32- (aq),NaOH過量使c(Na+)增大,上述平衡逆向移動.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氧化鎂與稀鹽酸反應:H++OH-═H2O | |
| B. | 氯化鋇溶液與硫酸鈉溶液反應:Ba2++SO42-═BaSO4↓ | |
| C. | FeCl3溶液中加入Fe粉:Fe3++Fe═2Fe2+ | |
| D. | 碳酸鈉溶液與足量醋酸反應:Na2CO3+2H+═2Na++CO2↑+H20 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
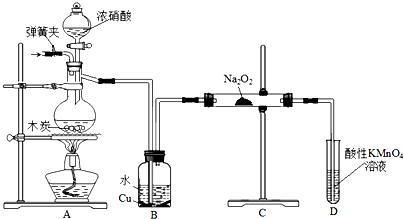
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
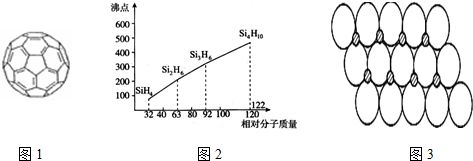
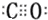 .
.
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
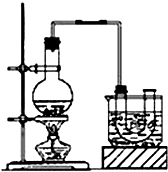 已知:CH3CH2OH+NaBr+H2SO4(濃)$\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.
已知:CH3CH2OH+NaBr+H2SO4(濃)$\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.查看答案和解析>>
科目:高中化學 來源:2016-2017學年浙江省高一上10月月考化學試卷(解析版) 題型:選擇題
混合氣體由CH4和N2組成,測得混合氣體在標準狀況下的密度為0.893g/L,則混合氣體中N2和CH4的體積之 比為
比為
A.1:2 B.1:4 C.2:1 D.4:1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com