
 電能與化學能之間的轉化具有重要的使用價值.
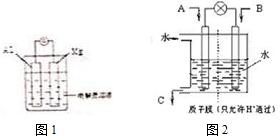
電能與化學能之間的轉化具有重要的使用價值.分析 (1)①當電解質溶液為稀硫酸時,Mg易失電子作負極、Al正極,負極鎂被氧化,正極上氫離子得電子發生還原反應;
②當電解質溶液為氫氧化鈉溶液時,該裝置能自發進行氧化還原反應,能構成原電池,Al作負極、Mg作正極;
(2)由反應方程式可知:CO+2H2=CH3OH,碳的化合價降低發生還原反應,正極上是氧氣發生得電子得還原反應;負極上二氧化硫失電子發生氧化反應,根據正極上電極反應式計算.
解答 解:(1)當電解質溶液為稀硫酸時,由于鎂、鋁都能與硫酸反應,且鎂比鋁活潑,則
①鋁為原電池的正極,發生還原反應,電極方程式為2H++2e-=H2↑,故答案為:正;2H++2e-=H2↑;
②Al為負極,發生氧化反應,電極方程式為2Al-6e-+8OH-=2AlO2-+4H2O,故答案為;負;2Al-6e-+8OH-=2AlO2-+4H2O;
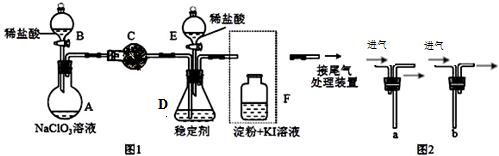
(2)由反應方程式可知:CO+2H2=CH3OH,碳的化合價降低發生還原反應,正極上是氧氣發生得電子得還原反應;負極上二氧化硫失電子發生氧化反應,若A為SO2,B為O2,C為H2SO4時,負極上二氧化硫失電子和水反應生成硫酸,電極反應式為:SO2+2H2O-2e-=4H++SO42-,故答案為:正;SO2+2H2O-2e-=4H++SO42-.
點評 本題考查原電池原理,為高頻考點,把握原電池的工作原理為解答的關鍵,側重電極、電極反應的考查,注意不能直接利用金屬活潑性判斷負極,應從氧化還原反應的角度考慮,題目難度不大.


科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 高溫有利于提高反應的轉化率 | |
| B. | 高溫可增大反應的限度 | |
| C. | 700K時反應催化劑活性最強,反應速率更快 | |
| D. | 高溫才可以自發向右進行 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
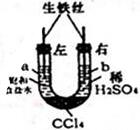 利用如圖裝置進行實驗,開始時,a、b兩處液面相平,密封好,放置一段時間.下列說法不正確的是( )
利用如圖裝置進行實驗,開始時,a、b兩處液面相平,密封好,放置一段時間.下列說法不正確的是( )| A. | a管發生吸氧腐蝕,b管發生析氫腐蝕 | |
| B. | 一段時間后,a管液面高于b管液面 | |
| C. | a處、b處溶液的pH都增大 | |
| D. | a、b兩處具有相同的電極反應式:Fe-3e-═Fe3+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在pH=1溶液中:NH4+、K+、ClO-、Cl- | |
| B. | 在含有大量CO32-溶液中:NH4+、Na+、Cl-、H+ | |
| C. | 有NO3-存在的強酸性溶液中:NH4+、Ba2+、Fe2+、Br- | |
| D. | 在強堿溶液中:Na+、K+、CO32-、SiO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH4+、Na+、Br-、SO42- | |
| B. | Al3+、Cl-、OH-、HCO3- | |
| C. | pH=0的溶液中:ClO-、SO42-、Fe2+、K+ | |
| D. | 由水電離的c(OH-)=10-14mol•L-1的溶液中:CH3COO-、SO42-、Na+、NH4+ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com