
 ij�ضȕr(sh��)����һ��(g��)2L�����]�����У�X��Y��Z���N���w�����|(zh��)�����S�r(sh��)�g��׃��������D��ʾ������(j��)�D�Д�(sh��)��(j��)��ԇ�(xi��)���пհף�
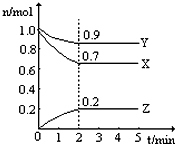
ij�ضȕr(sh��)����һ��(g��)2L�����]�����У�X��Y��Z���N���w�����|(zh��)�����S�r(sh��)�g��׃��������D��ʾ������(j��)�D�Д�(sh��)��(j��)��ԇ�(xi��)���пհף����� ����(j��)�D��֪���S������(y��ng)�M(j��n)�У�X��Y�����|(zh��)�����p�ٶ�Z���|(zh��)���������f(shu��)��X��Y�Ƿ���(y��ng)���Z�������
��1���_(d��)��ƽ���B(t��i)�r(sh��)�����ӷ���(y��ng)�ġ�n��X��=��1.0-0.7��mol=0.3mol����n��Y��=��1.0-0.9��mol=0.1mol����n��Z��=��0.2-0��mol=0.2mol��ͬһ����(y��ng)��ͬһ�r(sh��)�g��(n��i)���ӷ���(y��ng)�ĸ����|(zh��)�����|(zh��)����֮�ȵ�����Ӌ(j��)����(sh��)֮�ȣ�����X��Y��Z��Ӌ(j��)����(sh��)֮��=0.3mol��0.1mol��0.2mol=3��1��2����(j��)�˕�(sh��)��(xi��)����ʽ��
��2��Z��ƽ������(y��ng)����=$\frac{\frac{��n}{V}}{��t}$��
��3����غ��ݗl���£����w�����|(zh��)����֮�ȵ����䉺��(qi��ng)֮�ȣ�
��4��X���D(zhu��n)����=$\frac{�D(zhu��n)����}{��ʼ��}$��100%Ӌ(j��)�㣮
��� �⣺����(j��)�D��֪���S������(y��ng)�M(j��n)�У�X��Y�����|(zh��)�����p�ٶ�Z���|(zh��)���������f(shu��)��X��Y�Ƿ���(y��ng)���Z�������
��1���_(d��)��ƽ���B(t��i)�r(sh��)�����ӷ���(y��ng)�ġ�n��X��=��1.0-0.7��mol=0.3mol����n��Y��=��1.0-0.9��mol=0.1mol����n��Z��=��0.2-0��mol=0.2mol��ͬһ����(y��ng)��ͬһ�r(sh��)�g��(n��i)���ӷ���(y��ng)�ĸ����|(zh��)�����|(zh��)����֮�ȵ�����Ӌ(j��)����(sh��)֮�ȣ�����X��Y��Z��Ӌ(j��)����(sh��)֮��=0.3mol��0.1mol��0.2mol=3��1��2������ԓ����(y��ng)����ʽ��3X+Y?2Z��
�ʴ𰸞飺3X+Y?2Z��
��2��Z��ƽ������(y��ng)����=$\frac{\frac{��n}{V}}{��t}$=$\frac{\frac{0.2}{2}}{2}$=0.05mol/��L��min�����ʴ𰸞飺0.05mol/��L��min����
��3������(j��)�D��֪��δ����(y��ng)�r(sh��)��Ϛ��w�����|(zh��)����=��1.0+1.0��mol=2.0mol��ƽ���B(t��i)��Ϛ��w���|(zh��)����=��0.9+0.7+0.2��mol=1.8mol����غ��ݗl���£����w�����|(zh��)����֮�ȵ����䉺��(qi��ng)֮�ȣ�����ƽ���B(t��i)�wϵ����(qi��ng)���_(k��i)ʼ�r(sh��)��$\frac{1.8mol}{2.0mol}$=0.9����
�ʴ𰸞飺0.9��
��4��X���D(zhu��n)����=$\frac{�D(zhu��n)����}{��ʼ��}$��100%=$\frac{1-0.7}{1}$��100%=30%���ʴ𰸞飺30%��
�c(di��n)�u(p��ng) ���}����D���������(c��)�ؿ���W(xu��)��������Ӌ(j��)�����������_����׃��څ��(sh��)���x�����|(zh��)����׃�����c��Ӌ(j��)����(sh��)���P(gu��n)ϵ���ɽ���y�c(di��n)�ǣ�3���}Ӌ(j��)�㣬�}Ŀ�y���еȣ�


 ��˼�S�������I(y��)��ټ��ִ�W(xu��)������ϵ�д�
��˼�S�������I(y��)��ټ��ִ�W(xu��)������ϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}

�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ��x���}
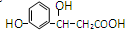 ���������l(f��)���ķ���(y��ng)����У��ټӳɣ���ˮ�⣻����ȥ�������������y�R������������ȡ������Ӿۣ���s�ۣ���������
���������l(f��)���ķ���(y��ng)����У��ټӳɣ���ˮ�⣻����ȥ�������������y�R������������ȡ������Ӿۣ���s�ۣ���������| A�� | �٢ݢ� | B�� | �٢ڢݢ� | C�� | �ڢޢ�� | D�� | �ڢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
| ��(sh��)�(y��n)���� | ��(sh��)�(y��n)�F(xi��n)�� |
| ����ɰ��Ħ������V���c��ˮ����(y��ng)������(y��ng) ��(y��ng)����Һ�еμӷ�̪ | A������ˮ�棬�۳�һ��(g��)С����ˮ���ϟo(w��)������ ��(d��ng)���S֮��ʧ����Һ׃�tɫ |
| ���c�c���з�̪ԇҺ����ˮ����(y��ng) | B���a(ch��n)�����w�����ڿ՚���ȼ������Һ׃�ɜ\�tɫ |
| ���V�l�c2mol•L-1���}�ᷴ��(y��ng) | C������(y��ng)��ʮ�֏�(qi��ng)�ң��a(ch��n)���o(w��)ɫ���w |
| ���X�l�c2mol•L-1���}�ᷴ��(y��ng) | D�����ҷ���(y��ng)���a(ch��n)���o(w��)ɫ���w |
| ����AlCl3��Һ�еμ�NaOH��Һ���^(gu��)�� | E�����ɰ�ɫ�z��������^��������ʧ |
| ��(sh��)�(y��n)���� | ��(sh��)�(y��n)�F(xi��n)���(xi��)��̖(h��o)�� |
| �� | B |
| �� | A |
| �� | D |
| �� | C |
| �� | E |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
 �ö������ȣ�ClO2�����F���c��Na2FeO4Ħ���|(zh��)����166g•mol-1�������̓�ˮ��������y(t��ng)�ă�ˮ��Cl2��(du��)��ˮ�M(j��n)�������dz������ˮ̎���¼��g(sh��)��ClO2��Na2FeO4��ˮ̎���^(gu��)���зքe��߀ԭ��Cl-��Fe3+��
�ö������ȣ�ClO2�����F���c��Na2FeO4Ħ���|(zh��)����166g•mol-1�������̓�ˮ��������y(t��ng)�ă�ˮ��Cl2��(du��)��ˮ�M(j��n)�������dz������ˮ̎���¼��g(sh��)��ClO2��Na2FeO4��ˮ̎���^(gu��)���зքe��߀ԭ��Cl-��Fe3+���鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ��x���}
| A�� | NaAlO2��Һ��ͨ���^(gu��)����CO2��2AlO2-+3H2O+CO2�T2Al��OH��3��+CO32- | |
| B�� | ���\��Һ�еμ�Ba��OH��2��Һ��SO42-��ȫ������Al3++Ba2++SO42-+3OH-�TBaSO4��+Al��OH��3�� | |
| C�� | 200 mL 2 mol/L��FeBr2��Һ��ͨ��11.2 L��(bi��o)��(zh��n)��r�µ��Ț⣺4Fe2++6Br-+5Cl2�T4Fe3++3Br2+10Cl- | |
| D�� | �ڏ�(qi��ng)�A��Һ�д������c�cFe��OH��3����(y��ng)����Na2FeO4��3ClO-+2Fe��OH��3�T2FeO42-+3Cl-+H2O+4H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ��x���}
 ���������Ƃ䰬�̲���ˎ���������������ԭ�ϣ���Y(ji��)��(g��u)��(ji��n)ʽ��D���������P(gu��n)��������f(shu��)�������_���ǣ�������
���������Ƃ䰬�̲���ˎ���������������ԭ�ϣ���Y(ji��)��(g��u)��(ji��n)ʽ��D���������P(gu��n)��������f(shu��)�������_���ǣ�������| A�� | ������ķ���ʽ��C7H9O6 | |
| B�� | 1mol�������c����NaOH��Һ����(y��ng)���������NaOH���|(zh��)������5mol | |
| C�� | 1 mol�������c�����c����(y��ng)����56L��� | |
| D�� | �������ܰl(f��)����ȥ����(y��ng)��Ҳ���c�Ҵ�������l(f��)��ȡ������(y��ng) |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ��x���}
| A�� | Li�����c(di��n)����Na�����c(di��n) | |
| B�� | CaF2���w��Ca2+�����(sh��)��4 | |
| C�� | �ɱ����w��ÿ��(g��)CO2������?ch��)����x����������CO2���Ӕ�(sh��)��10��(g��) | |
| D�� | SiO2 �ľ��w����С�h(hu��n)�ϵ�ԭ�ӂ�(g��)��(sh��)��6��(g��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ��x���}
| A�� | 4 g�����к��еķ��Ӕ�(sh��)��ԭ�Ӕ�(sh��)����NA | |
| B�� | ��(bi��o)��(zh��n)��r�£�22.4 L CCl4�к��еķ��Ӕ�(sh��)��NA | |
| C�� | 1 L 0.1 mol•L-1�Ҵ���Һ�к��е���ԭ�Ӕ�(sh��)��0.1NA | |
| D�� | 1 mol Cl2��ȫ����(y��ng)�D(zhu��n)�Ƶ���Ӕ�(sh��)һ����2NA |
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o(w��)���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com