
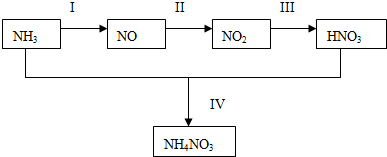
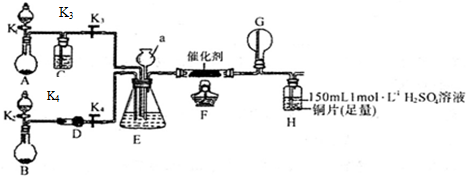
分析 NH3經一系列反應得到HNO3和NH4NO3的過程,氨氣的催化氧化生成一氧化氮,一氧化氮和空氣中氧氣反應生成二氧化氮,二氧化氮溶于水生成硝酸和一氧化氮,氨氣和硝酸反應生成硝酸銨,裝置圖中A、B分別用于制備氧氣和氨氣,由裝置可知A應用于制備氧氣,C為干燥裝置,可為濃硫酸,B為制備氨氣裝置,可用濃氨水和NaOH固體制備,D為干燥氨氣裝置,在F中發生氧化還原反應生成NO,G中可生成二氧化氮氣體,二氧化氮和水在H中反應生成硝酸,可氧化銅,生成的NO不能直接排放到空氣中,應有尾氣處理裝置.
①由裝置圖可知裝置A用于制備氧氣,可由過氧化氫在二氧化錳催化作用下制備,E可用于混合物氧氣和氨氣,因氨氣易溶于水,注意不能用水溶液;
②成功模擬了過程Ⅱ的反應,說明生成二氧化氮氣體,顏色為紅棕色,H中的溶液變成藍色,說明硝酸氧化銅生成銅離子,欲使H裝置中所得溶液為純凈的CuSO4溶液,根據硫酸的物質的量可確定被氧化的銅的物質的量,結合N原子守恒計算消耗硝酸的物質的量,進而計算氨氣的物質的量和體積;
(3)使G處圓底燒瓶中產生大量白煙,應通入氨氣和硝酸反應;
(4)裝置缺少尾氣處理.
解答 解:裝置圖中A、B分別用于制備氧氣和氨氣,由裝置可知A應用于制備氧氣,C為干燥裝置,可為濃硫酸,B為制備氨氣裝置,可用濃氨水和NaOH固體制備,D為干燥氨氣裝置,在F中發生氧化還原反應生成NO,G中可生成二氧化氮氣體,二氧化氮和水在H中反應生成硝酸,可氧化銅,生成的NO不能直接排放到空氣中,應有尾氣處理裝置.
①由裝置圖可知裝置A用于制備氧氣,可由過氧化氫在二氧化錳催化作用下制備,反應的方程式為2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑,E可用于混合物氧氣和氨氣,控制通入氨氣和氧氣的體積比、平衡裝置內的壓強,因氨氣易溶于水,則不能用水溶液,故d錯誤,
故答案為:2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑;d;
②成功模擬了過程Ⅱ的反應,說明生成二氧化氮氣體,顏色為紅棕色,H中的溶液變成藍色,說明硝酸氧化銅生成銅離子,反應的離子方程式為3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,n(H2SO4)=0.15L×1mol/L=0.15mol,則n(CuSO4)=0.15mol,需要0.15molCu,則由3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O可知需要0.1molHNO3,由N原子守恒可知需要0.1mol氨氣,體積為0.1mol×22.4L/mol=2.24L,
故答案為:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;2.24L;
(3)使G處圓底燒瓶中產生大量白煙,應通入氨氣和硝酸反應,因A制備氧氣,B制備氨氣,則關閉K3并熄滅酒精燈,故答案為:a;
(4)最后生成的NO不能直接排放到空氣中,為防止污染空氣,應有尾氣處理裝置,故答案為:缺少尾氣處理裝置.
點評 本題考查了氨氣制備及化學性質,為高考常見題型,題目難度中等,注意掌握氨氣的制備原理及具有的化學性質,根據題干信息明確實驗目的及反應原理為解答關鍵,試題有利于培養學生的分析、理解能力及化學實驗能力.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
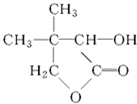 G的合成路線如圖:
G的合成路線如圖: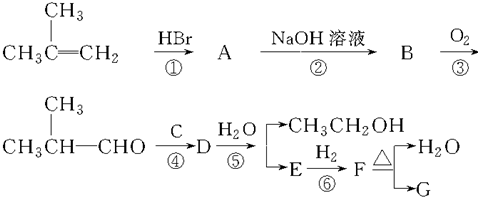
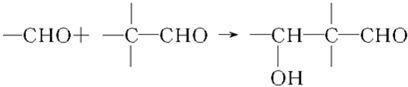
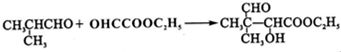
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二氧化硅溶于水顯酸性,所以二氧化硅屬于酸性氧化物 | |
| B. | 二氧化硅是酸性氧化物,它不溶于任何酸 | |
| C. | 二氧化碳通入水玻璃可以得到硅酸 | |
| D. | 因為高溫時二氧化硅與碳酸鈉反應放出二氧化碳,所以硅酸的酸性比碳酸強 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
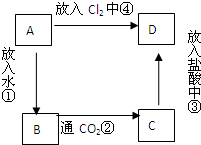 物質A是由A元素組成的單質,將其在酒精燈火焰上灼燒,火焰為黃色,B,C,D是含有A元素的三種不同化合物,A、B、C、D按圖關系進行轉化:
物質A是由A元素組成的單質,將其在酒精燈火焰上灼燒,火焰為黃色,B,C,D是含有A元素的三種不同化合物,A、B、C、D按圖關系進行轉化:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 弱酸 | CH3COOH | H2CO3 | HNO2 |
| 電離常數 | K=1.8×10-5 | K=4.3×10-7 K=5.6×10-11 | K=5.0×10-4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 還原劑是HCl,氧化劑是MnO2 | |
| B. | 每消耗1mol MnO2,轉移電子的物質的量為2 mol | |
| C. | 每轉移1mol電子,則可以制得標況下Cl2 22.4L | |
| D. | 生成的Cl2中,除含有一些水蒸氣外,還含有HCl雜質 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com