
| A. | 0.1mol•L-1氨水中,c(OH-)=c(NH4+) | |
| B. | 10 mL 0.02mol•L-1HCl溶液與10 mL 0.02mol•L-1Ba(OH)2溶液充分混合,若混合后溶液的體積為20 mL,則溶液的pH=12 | |
| C. | 在0.1mol•L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+) | |
| D. | 0.1mol•L-1某二元弱酸強堿鹽NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A) |
分析 A.氨水中主要成分是NH3•H2O,NH3•H2O是一元弱堿,電離產生NH4+和OH-,H2O也電離出OH-;
B.計算混合后的c(OH-),再計算溶液的pH;
C.將物料守恒關系式代入電荷守恒關系式即可解答;
D.根據NaHA化學式,溶液中Na+濃度等于含A元素微粒濃度和.
解答 解:A.氨水中主要成分是NH3•H2O,NH3•H2O是一元弱堿,電離產生NH4+和OH-,H2O也電離出OH-,則c(NH4+)<c(OH-),故A錯誤;
B.10ml0.02mol/L的HCl溶液與10ml0.02mol/L的Ba(OH)2溶液充分混合后,若混合后溶液體積為20ml,反應后的溶液中C(OH-)c(OH-)=$\frac{0.04mol/L×0.01L-0.02mol/L×0.01L}{0.02L}$=0.01 mol•L-1,c(H+)=$\frac{1×1{0}^{-14}}{0.01}$=10-12mol/L,則pH等于12,故B正確;
C.溶液中存在的陽離子是:H+、Na+,陰離子是:OH-、CH3COO-,根據電荷守恒有:①C(H+)+C(Na+)=C(OH-)+C(CH3COO-),依據醋酸根(碳元素守恒)寫出物料守恒關系得:C(Na+)=C(CH3COO-)+C(CH3COOH)②;將②代入①可得:c(OH-)=c(CH3COOH)+c(H+),故C正確;
D.A元素的存在形式為:A2-、HA-、H2A,根據物料守恒,NaHA中,c(Na+):c(含A微粒)=1:1,0.1mol•L-1某二元弱酸強堿鹽NaHA溶液中,c(Na+)=c(A2-)+c(HA-)+c(H2A),故D錯誤;
故選BC.
點評 本題考查了弱電解質的電離、pH計算及鹽類水解等知識,要考慮電離和水解,注意物料守恒、水解守恒的應用,題目難度中等.


科目:高中化學 來源: 題型:選擇題
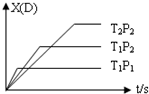 已知可逆反應 mA(g)+nB(g)?pC(g)+qD(g),反應中D的物質的量分數X(D)與時間t的關系如圖,則下列敘述正確的是( )
已知可逆反應 mA(g)+nB(g)?pC(g)+qD(g),反應中D的物質的量分數X(D)與時間t的關系如圖,則下列敘述正確的是( )| A. | 正反應為放熱反應 | B. | m+n>p+q | ||
| C. | T1<T2 | D. | P1<P2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 組別 | 鎂鋁合金質量.mg | HCl物質的量/mol | 氫氣的體積/mL |
| 甲 | 255 | X | 280 |
| 乙 | 385 | X | 336 |
| 丙 | 459 | X | 336 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 有機物 | 氫氧化鈉 | 銀氨溶液 | 新制氫氧化銅 | 金屬鈉 |
| A | 發生中和反應 | 不反應 | 溶解 | 放出氫氣 |
| B | 不反應 | 發生銀鏡反應 | 生成紅色沉淀 | 放出氫氣 |
| C | 發生水解反應 | 發生銀鏡反應 | 生成紅色沉淀 | 不反應 |
| D | 發生水解反應 | 不反應 | 不反應 | 不反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 改變某一條件,使v(正)、v(逆)均改變,化學平衡一定移動 | |
| B. | 改變某一條件,使v′(正)>v′(逆)不變,化學平衡一定逆向移動 | |
| C. | 改變某一條件,使v′(正)增大,v′(逆)不變,化學平衡一定正向移動 | |
| D. | 改變某一條件后,v′(正)、v′(逆)同時增大或同時減小時,化學平衡不移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | +3 | B. | +2 | C. | -2 | D. | +1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 向溶液乙中滴加KSCN溶液,溶液顏色變紅,則原礦石樣品中存在Fe3+ | |
| B. | 向溶液乙中滴加少量氫氧化鈉溶液,一定出現紅褐色沉淀 | |
| C. | 向溶液甲中滴加KSCN溶液,溶液顏色變紅,則原礦石樣品中存在Fe3+ | |
| D. | 該礦石一定為赤鐵礦 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com