
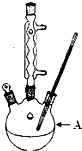
 “酒是陳的香”,是因為酒在儲存過程中生成了有香味的乙酸乙酯.在實驗室我們可以用如圖所示的裝置來制取乙酸乙酯.回答下列問題:
“酒是陳的香”,是因為酒在儲存過程中生成了有香味的乙酸乙酯.在實驗室我們可以用如圖所示的裝置來制取乙酸乙酯.回答下列問題: CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.分析 (1)由裝置圖可知儀器A的名稱分液漏斗;C球形干燥管的管口伸入液面下可能發生倒吸,同時起冷凝作用;
(2)液體加熱要加碎瓷片,防止暴沸;乙酸與乙醇在濃硫酸作用下加熱發生酯化反應生成乙酸乙酯和水,該反應為可逆反應;
(3)制備乙酸乙酯時常用飽和碳酸鈉溶液吸收乙酸乙酯,乙醇溶解,碳酸鈉與乙酸反應除去乙酸、同時降低乙酸乙酯的溶解度,便于分層;
(4)乙酸與乙醇在濃硫酸作用下加熱發生酯化反應生成乙酸乙酯和水,該反應為可逆反應,不可能反應到底,據此分析.
解答 解:(1)由裝置圖可知儀器A的名稱分液漏斗;C球形干燥管的管口伸入液面下可能發生倒吸,球形干燥管體積大,可以防止倒吸,同時起冷凝作用,
故答案為:分液漏斗;防止倒吸;
(2)液體加熱要加碎瓷片,引入汽化中心,可防止溶液暴沸,乙酸與乙醇在濃硫酸作用下加熱發生酯化反應生成乙酸乙酯和水,同時該反應可逆,反應的化學方程式為CH3COOH+CH3CH2OH CH3COOC2H5+H2O,
CH3COOC2H5+H2O,
故答案為:防止暴沸;CH3COOH+HOCH2CH3 CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(3)制備乙酸乙酯時常用飽和碳酸鈉溶液吸收乙酸乙酯,目的是除去粗產品的乙酸、乙醇,降低酯在其中的溶解度小,有利于酯的分離,
故答案為:飽和碳酸鈉溶液;除去粗產品的乙酸、乙醇,降低酯在其中的溶解度小,有利于酯的分離;
(4)該實驗中,若用3mol乙醇和1mol乙酸在濃硫酸作用下加熱,充分反應后,不能生成1mol乙酸乙酯,因為生成乙酸乙酯的反應是可逆反應,1mol乙酸不能完全變成生成物,故答案為:不能;該反應是可逆反應,反應不能進行到底.
點評 本題考查乙酸乙酯的制備,注意飽和碳酸鈉溶液的作用以及酯化反應的機理,難度適中,注重基礎知識的考查.


科目:高中化學 來源:2016-2017學年寧夏衛一高一上10月月考化學a卷(解析版) 題型:選擇題
關于分液漏斗的使用,下列說法正確的是
A.可在分液漏斗內用四氯化碳萃取碘酒中的碘單質
B.放出下層液體時,應打開上方的玻璃塞,并使下端管口緊貼燒杯內壁
C.在分液漏斗中加入萃取劑后應上下顛倒搖勻使萃取劑與溶質充分接觸
D.分液漏斗在使用前只需檢查旋塞芯處是否漏水即可
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 苯甲酸廣泛應用于制藥和化工行業,某興趣小組同學利用高錳酸鉀氧化甲苯制備苯甲酸(KMnO4中性條件下還原產物為MnO2,酸性條件下為Mn2+)
苯甲酸廣泛應用于制藥和化工行業,某興趣小組同學利用高錳酸鉀氧化甲苯制備苯甲酸(KMnO4中性條件下還原產物為MnO2,酸性條件下為Mn2+)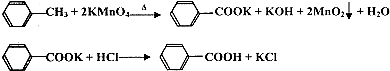
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 體積(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該反應為可逆反應,不可能進行到底,即乙醇的轉化率一定達不到100% | |
| B. | 乙酸揮發,導致其量減少,乙醇過量,不能充分轉化為乙酸乙酯 | |
| C. | 產物不穩定,易被氧化為其他物質而影響乙醇的轉化率 | |
| D. | 餾出物導入飽和碳酸鈉溶液液面上,有較多的乙酸乙酯溶解于水溶液中 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
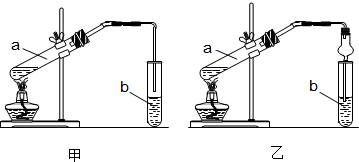
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| NaOH溶液 | 銀氨溶液 | 新制Cu(OH)2 | 金屬鈉 | |
| A | 發生中和反應 | 不反應 | 溶解 | 生成氫氣 |
| B | 不反應 | 有銀鏡反應 | 有紅色沉淀 | 放出氫氣 |
| C | 發生水解反應 | 有銀鏡反應 | 有紅色沉淀 | 不反應 |
| D | 發生水解反應 | 不反應 | 不反應 | 不反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
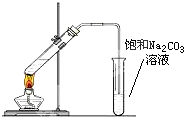 實驗室可以用圖所示的裝置制取乙酸乙酯.回答下列問題:
實驗室可以用圖所示的裝置制取乙酸乙酯.回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com