
分析 (1)純堿中碳酸鈉與稀鹽酸反應放出二氧化碳,根據HCl的質量,根據反應的化學方程式,計算出二氧化碳、純堿中碳酸鈉的質量和反應后溶液中溶質氯化鈉的質量;
(2)根據“溶質質量分數=$\frac{溶質質量}{溶液質量}$×100%”,計算出反應后所得溶液中溶質的質量分數計算.
解答 解:設參加反應的Na2CO3質量為x,生成的NaCl的質量為y,生成二氧化碳的質量為z.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 117 44
x 14.6g y z
$\frac{106}{x}=\frac{73}{14.62}=\frac{117}{y}=\frac{44}{z}$
解之得 x=21.2g,y=23.4g,z=8.8g
純堿樣品中NaCl的質量=22.8g-21.2g=1.6g
反應后溶液中NaCl的質量為=23.4g+1.6g=25g
反應后溶液中NaCl的質量分數=$\frac{25g}{200g}$×100%=12.5%
答:(1)該純堿樣品中Na2CO3的質量21.2g;
(2)所得溶液中溶質的質量分數為12.5%.
點評 反應后所得溶液中溶質氯化鈉由原粉末中所含的氯化鈉與反應后生成的氯化鈉兩部分所組成,解題時要注意到這點.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題

| 序號 | 實驗步驟 | 預期現象 | 結論 |
| 1 | |||
| 2 | 錐形瓶中液體含大量Br- | ||
| 3 | 錐形瓶中液體含大量H+ |

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3CH2CH2OH+HBr$→_{H+}^{△}$CH3CH2CH2Br+H2O | |
| B. |  +NaHCO3→ +NaHCO3→ +H2CO3 +H2CO3 | |
| C. |  +CO2+H2O→ +CO2+H2O→ +NaHCO3 +NaHCO3 | |
| D. |  +3Br2→ +3Br2→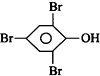 ↓+3HBr ↓+3HBr |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 蔗糖、麥芽糖互為同分異構體 | |
| B. | 常用蛋白質的顏色反應來鑒別部分蛋白質 | |
| C. | 用Na2CO3溶液不能區分CH3COOH和CH3COOCH2CH3 | |
| D. | 油脂在酸性或堿性條件下均能發生水解反應,且產物不同 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

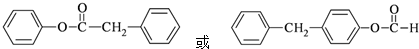 .
. $→_{Pd/C}^{H_{2}}$
$→_{Pd/C}^{H_{2}}$ .化合物
.化合物  是合成抗癌藥物美發倫的中間體,請寫出以
是合成抗癌藥物美發倫的中間體,請寫出以  和
和 為原料制備該化合物的合成路線流程圖(無機試劑任用).合成路線流程圖示例如下:
為原料制備該化合物的合成路線流程圖(無機試劑任用).合成路線流程圖示例如下:查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 )結構
)結構 

 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com