
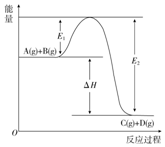
 反應A(g)+B(g)═C(g)+D(g)過程中的能量變化如圖所示,回答下列問題.
反應A(g)+B(g)═C(g)+D(g)過程中的能量變化如圖所示,回答下列問題.分析 (1)根據反應物與生成物總能量大小判斷;
(2)由圖象可知E1表示反應物斷鍵吸收的總能量,E2表示生成物形成放出的總能量,△H=反應物斷鍵吸收的總能量-生成物形成放出的總能量;
(3)加入催化劑能降低反應的活化能,催化劑不改變反應物總能量與生成物總能量之差即反應熱不變;
(4)加入催化劑能降低反應的活化能.
解答 解:(1)由圖象可知該反應是一個能量降低的反應,所以屬于放熱反應;故答案為:放熱;
(2)由圖象可知E1表示反應物斷鍵吸收的總能量,E2表示生成物形成放出的總能量,△H=反應物斷鍵吸收的總能量-生成物形成放出的總能量=E1-E2;
故答案為:反應物斷鍵吸收的總能量;生成物形成放出的總能量;E1-E2;
(3)加入催化劑改變了反應的途徑,降低反應所需的活化能,但反應熱取決于反應物總能量與生成物總能量之差,與催化劑的使用無關,所以加入催化劑對反應熱無影響,故答案為:無影響,因為反應熱取決于反應物總能量與生成物總能量的差值,與催化劑無關;
(4)加入催化劑能降低反應的活化能,所以E1和E2均減小;故答案為:減小;減小.
點評 本題考查反應熱的判斷,影響反應熱和平衡的因素,難度適中,注意催化劑對活化能和反應熱的影響.


科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 同溫、同壓下,相同質量的氣體都占有相同的體積 | |
| B. | 同溫、同壓下,相同體積的氣體都含有相同數目的原子 | |
| C. | 在任何情況下,1 mol CO2和64 g SO2所含有分子數和原子總數都相同 | |
| D. | 1 mol某氣體的體積約為22.4 L,該氣體所處的狀況一定是標準狀況 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 18g H2O在標準狀況下的體積是22.4L | |
| B. | 常溫常壓下,4g H2含有的分子數為 2NA | |
| C. | 2.3g金屬鈉變為鈉離子時失去的電子數為NA | |
| D. | 17g氨氣所含原子數目為3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
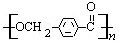 的路線:
的路線: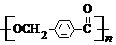
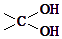 →
→ ═O+H2O
═O+H2O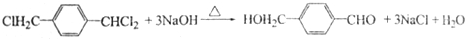 ;該反應過程中生成的不穩定中間體的結構簡式應是
;該反應過程中生成的不穩定中間體的結構簡式應是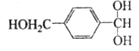 .
.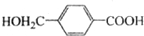 ,D的同分異構體中含有苯環且水解產物之一為乙酸的有3種,寫出其中的一種結構簡式:
,D的同分異構體中含有苯環且水解產物之一為乙酸的有3種,寫出其中的一種結構簡式: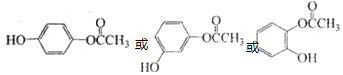 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 跟水反應時,水作氧化劑 | B. | NaH在水中顯酸性 | ||
| C. | 跟液氨反應時,有NaNH2生成 | D. | 跟乙醇反應時,NaH被氧化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 小蘇打溶液和NaAlO2溶液反應可以產生沉淀和氣體,可以用作泡沫滅火器成分 | |
| B. | 侯德榜制堿過程涉及溶解度差異的原理,工業上從鋁土礦制備較高純度Al2O3的主要工藝流程中使用到CO2氣體 | |
| C. | 一定條件下,Na、Mg、Fe都能和水反應生成對應的堿和氫氣,Na2O2、MgO、Fe3O4都是堿性氧化物 | |
| D. | 納米Fe、納米Cu的化學活性都比原來增強,兩者都能與鹽酸反應生成氫氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
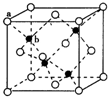 E、G、M、Q、T是五種原子序數依次增大的前四周期元素E、G、M是位于P區的同一周期的元素,M的價層電子排布為nsnnp2n,E與M原子核外的未成對電子數相等;QM2與QM2-為等電子體;T為過渡元素,其原子核外沒有未成對電子.請回答下列問題:
E、G、M、Q、T是五種原子序數依次增大的前四周期元素E、G、M是位于P區的同一周期的元素,M的價層電子排布為nsnnp2n,E與M原子核外的未成對電子數相等;QM2與QM2-為等電子體;T為過渡元素,其原子核外沒有未成對電子.請回答下列問題: (若有配位鍵,請用“→”表示),E、M電負性相差1.0,由此可以判斷EM應該為極性較強的分子,但實際上EM分子的極性極弱,請解釋其原因從電負性分析,CO中的共用電子對偏向氧原子,但分子中形成配位鍵的電子對是由氧原子單方面提供的,抵消了共用電子對偏向O而產生的極性;
(若有配位鍵,請用“→”表示),E、M電負性相差1.0,由此可以判斷EM應該為極性較強的分子,但實際上EM分子的極性極弱,請解釋其原因從電負性分析,CO中的共用電子對偏向氧原子,但分子中形成配位鍵的電子對是由氧原子單方面提供的,抵消了共用電子對偏向O而產生的極性; 查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com