
| A. | 5:3 | B. | 3:1 | C. | 1:1 | D. | 2:3 |
分析 設NaNO2的物質的量為xmol,NaNO3的物質的量為ymol,
2NO2+Na2CO3═NaNO2+NaNO3+CO2
2y y y y
NO+NO2+Na2CO3═2NaNO2 +CO2
$\frac{x-y}{2}$$\frac{x-y}{2}$ x-y $\frac{x-y}{2}$
已知產生22.4L(標準狀況下)CO2,則x+$\frac{x-y}{2}$$\frac{22.4L}{22.4L/mol}$=$\frac{22.4L}{22.4L/mol}$
溶液增加的質量為:2y•46+$\frac{x-y}{2}$•30+$\frac{x-y}{2}$•46-(y+$\frac{x-y}{2}$)•44=44,據此計算.
解答 解:設NaNO2的物質的量為xmol,NaNO3的物質的量為ymol,
2NO2+NaCO3═NaNO2+NaNO3+CO2
2y y y y
NO+NO2 +Na2CO3 ═2NaNO2 +CO2
$\frac{x-y}{2}$$\frac{x-y}{2}$ x-y $\frac{x-y}{2}$
已知產生22.4L(標準狀況下)CO2,則y+$\frac{x-y}{2}$=$\frac{22.4L}{22.4L/mol}$
溶液增加的質量為:2y•46+$\frac{x-y}{2}$•30+$\frac{x-y}{2}$•46-$\frac{22.4L}{22.4L/mol}$•44=44,
聯立兩個方程式解得:x:y=5:3,
所以吸收液中NaNO2和NaNO3的物質的量之比為5:3;
故選A.
點評 本題考查化學實驗基本操作、關系式計算等,題目難度中等,題目的計算量較大,是對學生分析能力、計算能力和綜合能力的考查.


科目:高中化學 來源: 題型:實驗題
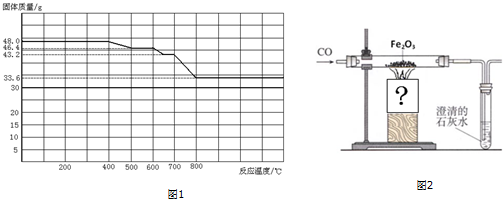
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②④⑥ | B. | ②④⑥ | C. | ①③⑤ | D. | ①②③⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 有單質生成的反應一定是氧化還原反應 | |
| B. | 在氧化還原反應中,非金屬單質一定是氧化劑 | |
| C. | 反應前后有元素化合價變化的反應一定是氧化還原反應 | |
| D. | 金屬陽離子被還原一定得到金屬單質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 負極是鋁失電子被氧化 | |
| B. | 電池工作時,電流由鋁電極沿導線流向鉑電極 | |
| C. | 以網狀的鉑為正極,可增大與氧氣的接觸面積 | |
| D. | 該電池通常只需更換鋁板就可繼續使用 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 苯丙醇胺的結構簡式為: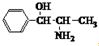 ,其分子中有2個手性碳原子 ,其分子中有2個手性碳原子 | |
| B. | 在NH4+和[Cu(NH3)4]2+中都存在配位鍵 | |
| C. | 完全由非金屬元素形成的化合物中也可能含有離子鍵 | |
| D. | CO2、SiO2都是分子晶體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 銅粉加入氯化鐵溶液中:Cu+Fe3+═Cu2++Fe2+ | |
| B. | 金屬鈉投到水中:Na+H2O═Na++OH-+H2↑ | |
| C. | 氫氧化鈉溶液加入到稀硫酸中:OH-+H+═H2O | |
| D. | 石灰石投入到稀鹽酸中:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com