
| 實驗裝置 | 現象 |
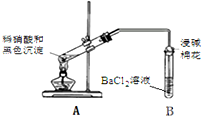 | 1.A試管中黑色沉淀逐漸溶解 2.A試管內上方出現紅棕色氣體 3.B試管中出現白色沉淀 |
分析 (1)將銅與濃硫酸反應后的溶液冷卻后通過過濾可以得到黑色固體;
(2)根據題中信息中檢驗銅離子的方法對②進行分析,然后得出正確結論;
(3)①紅棕色氣體為二氧化氮,說明稀硝酸被還原生成一氧化氮,黑色固體具有還原性;
②根據反應現象③可知黑色固體與稀硝酸反應生成了二氧化硫,證明黑色固體中含有硫元素;二氧化氮、二氧化硫的混合氣體能夠與氯化鋇反應生成硫酸鋇沉淀,據此寫出反應的離子方程式;
③還需要確定黑色固體中含有銅離子;
(4)濃硫酸具有強氧化性,能夠將硫化銅中硫氧化成硫酸銅、二氧化硫和水,據此寫出反應的化學方程式.
解答 解:(1)步驟Ⅲ中,“從反應后的混合物中分離出黑色沉淀”的操作為:將反應后的混合物倒入裝有冷水的燒杯中,冷卻后過濾,
故答案為:將反應后的混合物倒入裝有冷水的燒杯中,冷卻后過濾;
(2)向試液中滴加K4[Fe(CN)6]溶液,若產生紅褐色沉淀,證明有Cu2+,根據②將黑色沉淀放入稀硫酸中,一段時間后,滴加K4[Fe(CN)6]溶液,未見紅褐色沉淀可知,黑色固體中一定不含CuO,
故答案為:黑色沉淀中不含有CuO;
(3)①A試管內上方出現紅棕色氣體,說明反應中有一氧化氮生成,證明了黑色固體具有還原性,在反應中被氧化,
故答案為:還原;
②根據反應現象③B試管中出現白色沉淀可知,白色沉淀為硫酸鋇,說明黑色固體中含有硫元素;發生反應的離子方程式為:NO2+SO2+Ba2++H2O═BaSO4↓+NO↑+2H+,
故答案為:B試管中出現白色沉淀;NO2+SO2+Ba2++H2O═BaSO4↓+NO↑+2H+;
③為確認黑色沉淀是“銅的硫化物”,還需檢驗黑色固體中含有銅離子,方法為:取冷卻后A裝置試管中的溶液,滴加K4[Fe(CN)6]溶液,若產生紅褐色沉淀,證明有Cu2+,說明黑色沉淀是銅的硫化物,
故答案為:取冷卻后A裝置試管中的溶液,滴加K4[Fe(CN)6]溶液,若產生紅褐色沉淀,證明有Cu2+,說明黑色沉淀是銅的硫化物;
(4)濃硫酸具有強氧化性,硫化銅與濃硫酸反應的化學方程式為:CuS+4H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+4SO2↑+4H2O,
故答案為:CuS+4H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+4SO2↑+4H2O.
點評 本題考查了濃硫酸的化學性質、性質實驗方案的設計,題目難度中等,試題涉及的題量稍大,知識點較多,理解題中信息是解題關鍵,如根據銅離子檢驗方法解答(3)③;試題側重考查學生的分析、理解能力及化學實驗能力.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1mol•L-1的溶液中Na+、SiO32-、I-、CO32- | |
| B. | 2%的氨水中Ag+、K+、F-、NO3- | |
| C. | pH=1的溶液中NH4+、Na+、SO42-、C17H35COO- | |
| D. | 0.1mol•L-1的NaHSO4溶液中K+、Fe2+、Cl-、CrO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 水由液態變為玻璃態,體積縮小 | |
| B. | 水由液態變為玻璃態,體積膨脹 | |
| C. | 玻璃態是水的一種特殊狀態晶體 | |
| D. | 玻璃態水是水分子在空間有規則排列形成的 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該反應的化學平衡常數表達式是K=$\frac{{c}^{2}(C)•{c}^{2}(D)}{c(A)•c(B)}$ | |
| B. | 若向平衡體系中加入少量生成物C,則正、逆反應速率均增大 | |
| C. | 增大該體系的壓強,A的轉化率增大 | |
| D. | 該條件下B的平衡轉化率是40% |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡總壓強(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡氣體總濃度(×10-3 mol•L-1) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將碳、氫元素符號省略,只表示分子中鍵的連接情況 | |
| B. | 每個拐點、交點、端點均表示有一個碳原子 | |
| C. | 每一條線段代表一個共價鍵,每個碳原子有四條線段,用四減去線段數即是氫原子數 | |
| D. | C=C、C≡C鍵等官能團中的“=”和“≡”也可以省略 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com