
 如圖是實驗室制取乙酸乙酯的裝置.請回答下列問題:
如圖是實驗室制取乙酸乙酯的裝置.請回答下列問題:分析 (1)濃硫酸起到了催化作用和吸水作用;
(2)加熱液體時加入碎瓷片時為了防止溶液暴沸飛濺;
(3)酯化反應的本質為酸脫羥基,醇脫氫,該反應生成乙酸乙酯和水,且為可逆反應;
(4)飽和碳酸鈉溶液與乙酸反應除去乙酸、同時降低乙酸乙酯的溶解度,便于分層;乙酸乙酯密度小于水.
解答 解:(1)乙酸與乙醇發生酯化反應,需濃硫酸作催化劑,該反應為可逆反應,濃硫酸吸水利于平衡向生成乙酸乙酯方向移動,濃硫酸的作用為催化劑,吸水劑,故答案為:催化劑;吸水劑;
(2)燒瓶中加入碎瓷片的目的是防止暴沸,故答案為:防止暴沸;
(3)酯化反應的本質為酸脫羥基,醇脫氫,乙酸與乙醇在濃硫酸作用下加熱發生酯化反應生成乙酸乙酯和水,該反應為可逆反應,化學方程式為CH3COOH+C2H5OH$?_{△}^{濃硫酸}$ CH3COOC2H5+H2O,故答案為:CH3COOH+HOCH2CH3$?_{△}^{濃硫酸}$ CH3COOCH2CH3+H2O
(4)制備乙酸乙酯時常用飽和碳酸鈉溶液,目的是中和揮發出來的乙酸,使之轉化為乙酸鈉溶于水中,便于聞乙酸乙酯的香味;溶解揮發出來的乙醇;降低乙酸乙酯在水中的溶解度,便于分層得到酯,乙酸乙酯的密度小于水,故在上層,故答案為:中和乙酸、溶解乙醇;降低乙酸乙酯的溶解度,有利于分層; 乙酸乙酯.
點評 本題考查了乙酸乙酯的制備,題目難度不大,涉及濃硫酸、飽和碳酸鈉溶液的作用以及酯化反應的機理,試題培養了學生分析、理解能力及靈活應用所學知識解決實際問題的能力.


科目:高中化學 來源: 題型:選擇題
| A. | 點燃鎂、鋁前應用砂紙打磨,除去表面的氧化膜 | |
| B. | 用砂紙打磨的鋁條,放在酒精燈上加熱至熔化,鋁會滴落下來 | |
| C. | 鐵在氧氣中燃燒的產物主要成分是Fe2O3 | |
| D. | 金屬單質在自然界中都以化合物存在,因為它們都有較強的還原性 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
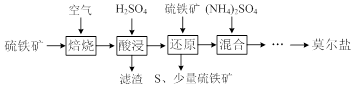
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

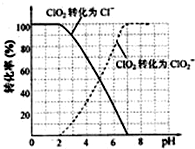
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 甲表示2molH2(g)所具有的能量一定比2mol氣態水所具有的能量多483.6KJ | |
| B. | 乙表示恒溫恒容條件下發生的可逆反應2NO2?N2O4(g)中,各物質的濃度與其消耗速率之間的關系,其中交點A對應的狀態為化學平衡狀態 | |
| C. | 丙表示A、B兩物質的溶解度隨溫度變化情況,將t1℃時的A、B飽和溶液分別由t1℃升溫至t2℃時,溶質的質量分數B>A | |
| D. | 丁表示常溫下,稀釋HA、HB兩種酸的稀溶液時,溶液pH隨加水量的變化,則同溫同濃度的HA溶液的pH小于HB溶液的pH |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 第15列元素原子的最外層電子排布為ns2 np5 | |
| B. | 只有第二列的元素原子最外層電子排布為ns2 | |
| C. | 第四周期第9列元素是鐵元素 | |
| D. | 第9列中元素中沒有非金屬元素 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com