
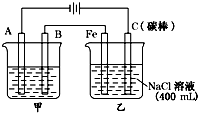
 如圖為相互串聯的甲乙兩電解池.試回答:
如圖為相互串聯的甲乙兩電解池.試回答:分析 圖示是兩個串聯的電解池,依據電源判斷A為陰極,B為陽極,Fe為陰極,C為陽極,
(1)電解精煉粗銅時,粗銅作陽極,純銅作陰極,電解質溶液為可溶性的銅鹽;
(2)乙池中是電解飽和食鹽水,溶液中的氫離子在陰極得到電子發生還原反應生成氫氣,破壞了水的電離平衡,氫氧根離子濃度增大;
(3)甲池是精煉銅,增重6.4g是銅的質量,根據電解反應過程中電極上的電子守恒計算.
解答 解:(1)電解精煉粗銅時,粗銅作陽極,純銅作陰極,電解質溶液為可溶性的銅鹽,根據圖片知,A是陰極,B是陽極,所以A極材料是純銅,陰極上銅離子得電子發生還原反應,電極反應式為:Cu2++2e-═Cu,B是陽極,電極材料是粗銅,陽極上銅失電子發生氧化反應,電極反應式為:Cu-2e-═Cu2+,電解質一般用可溶性的硫酸銅溶,
故答案為:陽;粗銅;Cu2++2e-═Cu;
(2)乙池中是電解飽和食鹽水,溶液中的氫離子在陰極得到電子發生還原反應生成氫氣,破壞了水的電離平衡,氫氧根離子濃度增大,遇少量石蕊試液變藍;
故答案為:藍;
(3)串聯電路中轉移電子相等,若甲槽陰極增重6.4g,由電極方程式Cu2++2e-═Cu可知,陰極上得到電子的物質的量=$\frac{6.4g}{64g/mol}$×2=0.2mol,乙槽陽極電極反應為:2Cl--2e-=Cl2↑,根據轉移電子相等得,放出氣體在標準狀況下的體積=$\frac{0.2mol}{2}$×22.4L/mol=2.24L,消耗氫離子也為0.2mol,所以剩余氫氧根為0.2mol,電解后得到堿液的物質的量濃度為$\frac{0.2mol}{0.4L}$=0.5mol/L
故答案為:2.24L;0.5mol/L.
點評 本題考查了電解池原理,為高頻考點,側重于學生的分析能力和計算能力的考查,明確陰陽極上發生的反應是解本題關鍵,再結合轉移電子相等分析解答,難度不大.


科目:高中化學 來源: 題型:多選題
| A. | 降低溫度 | B. | 增大容器體積 | C. | 升高溫度 | D. | 選用高效催化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫時,NaNO2溶液的pH=8,則該溶液中c(Na+)-c(NO2-)=9.9×10-7mol•L-1 | |
| B. | NaHSO4溶液與Ba(OH)2溶液反應至中性的離子方程式為:H++SO42++Ba2++OH-═BaSO4↓+H2O | |
| C. | 常溫下物質的量濃度相等的下列四種溶液:①NH4HSO4;②CH3COONH4;③NH4Cl;④NH4Fe(SO4)2,四種溶液中c(NH4+)比較:②>①>④>③ | |
| D. | 常溫下$\frac{Kw}{c({H}^{+})}$=1×10-10mol•L-1的溶液:Na+、K+、SiO32-、NO3-可以常量共存 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
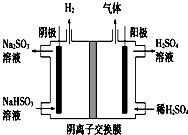 工業上用Na2SO3吸收尾氣中的SO2,再用如圖裝置電解(惰性電極)NaHSO3制取H2SO4,陰極電極反應式2H++2e-=H2↑,陽極區逸出氣體的成分為O2 SO2(填化學式).
工業上用Na2SO3吸收尾氣中的SO2,再用如圖裝置電解(惰性電極)NaHSO3制取H2SO4,陰極電極反應式2H++2e-=H2↑,陽極區逸出氣體的成分為O2 SO2(填化學式).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向某溶液中加入鹽酸酸化的氯化鋇溶液有白色沉淀生成,該溶液中一定含SO42- | |
| B. | 向蛋白質溶液中加入硫酸銅溶液,將得到的沉淀分離出來,再加水可重新溶解 | |
| C. | 除去苯中含有的苯酚,可先加NaOH溶液,充分反應后靜置分液 | |
| D. | 淀粉和稀硫酸混合加熱一段時間后,加入氫氧化鈉使溶液呈堿性,再加入新制Cu(OH)2后加熱,若有磚紅色沉淀生成,則淀粉已經完全水解 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
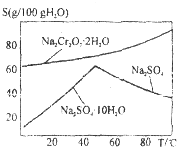 工業上以鉻鐵礦(主要成分FeO•Cr2O3)、碳酸鈉、氧氣和硫酸為原料生產重鉻酸鈉(Na2Cr2O7•2H2O)的主要反應如下:
工業上以鉻鐵礦(主要成分FeO•Cr2O3)、碳酸鈉、氧氣和硫酸為原料生產重鉻酸鈉(Na2Cr2O7•2H2O)的主要反應如下:查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 ;
; 結構(含E)的有13種;E的另一種同分異構體能發生銀鏡反應,能與足量金屬鈉生成氫氣,不能發生消去反應,其結構簡式為
結構(含E)的有13種;E的另一種同分異構體能發生銀鏡反應,能與足量金屬鈉生成氫氣,不能發生消去反應,其結構簡式為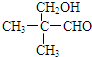 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com