
用酸性氫氧燃料電池為電源進行電解的實驗裝置如圖所示,下列說法正確的是(  )
)
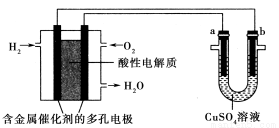
A.燃料電池工作時,正極反應為O2+2H2O+4e-=4OH-
B.電解精煉銅時,若轉移1mol電子,a極質量減少32g
C.鐵表面鍍銅時,a為鐵,b為Cu,工作一段時間要使右池溶液復原可加入適量的CuO
D.若a、b兩極均為石墨時,在相同條件下,a極產生的氣體與電池中消耗的O2體積相同
科目:高中化學 來源:2016-2017學年寧夏高二上月考二化學卷(解析版) 題型:選擇題
某溫度時,BaSO4在水中的沉淀溶解平衡曲線如下圖所示。下列說法正確的是( )
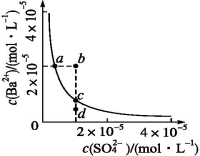
提示:BaSO4(s) 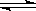 Ba2+(aq)+SO42-(aq)的平衡常數Ksp=c(Ba2+)·c(SO42-),稱為溶度積常數。
Ba2+(aq)+SO42-(aq)的平衡常數Ksp=c(Ba2+)·c(SO42-),稱為溶度積常數。
A.加入Na2SO4可以使溶液由a點變到b點
B.通過蒸發可以使溶液由d點變到c點
C.d點無BaSO4沉淀生成
D.a點對應的Ksp大于c點對應的Ksp
查看答案和解析>>
科目:高中化學 來源:2017屆遼寧省沈陽東北育才學校高三上期中模擬化學卷(解析版) 題型:選擇題
下列反應的離子方程式正確的是( )
A.用石墨作電極電解AlC13溶液:2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
B.酸性高錳酸鉀溶液與H2O2溶液混合:2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6 H2O
H2O
C.向NaHSO4溶液中滴加Ba(OH)2溶液至不再產生沉淀:
Ba2++OH-+H++SO42-=BaSO4↓+H2O
D.向Ca(HCO3)2溶液中加入足量Ca(OH)2的溶液:
Ca2++2HCO3-+2OH-=2H2O+CaCO3↓+CO32-
查看答案和解析>>
科目:高中化學 來源:2017屆江西省高三上11.27周考化學卷(解析版) 題型:選擇題
下列實驗設計能完成或實驗結論合理的是
A.證明一瓶紅棕色氣體是溴蒸氣還是二氧化氮,可用濕潤的碘化鉀-淀粉試紙檢驗,觀察試紙顏色的變化
B.鋁熱劑溶于足量稀鹽酸再滴加KSCN溶液,未出現血紅色,鋁熱劑中一定不含Fe2O3
C.測氯水的pH,可用玻璃棒蘸取氯水點在pH試紙上,待其變色后和標準比色卡比較
D.用核磁共振氫譜圖鑒別1-丙醇和2-丙醇
查看答案和解析>>
科目:高中化學 來源:2017屆江西省高三上月考三化學卷(解析版) 題型:實驗題
硫酸亞錫(SnSO4)是一種重要的硫酸鹽,主要用于電鍍工業的鍍錫、鋁合金表面的氧化著色、印染工業的媒染劑、雙氧水去除劑等。已知:酸性條件下,錫在水溶液中有Sn2+、Sn4+兩種主要存在形式,Sn2+易水解,易被氧化。某研究小組設計SnS O4制備路線如下:
O4制備路線如下:

請回答下列問題:
(1)SnCl2粉末需加濃鹽酸進行溶解,這樣操作的原因是 ;
(2)反應I得到的沉淀是SnO,得到該沉淀的離子方程式是 ;
(3)在反應I得到沉淀SnO后,要進行“過濾”、“漂洗”,檢驗SnO是否洗滌干凈的操作是 ;
(4)反應II之后的“操作”依次為 、 、過濾、洗滌、低溫干燥;
(5)某化學興趣小組對用于微電子器件生產的錫粉進行了純度測定:①取1.19 g試樣溶于稀硫酸中(雜質不參與反應),使Sn完全轉化為Sn2+;②加入過量的Fe2(SO4)3溶液;③用0 .2000 mol/L 酸性K2Cr2O7溶液滴定(產物中Cr呈+3價)至終點,消耗K2Cr2O7溶液15.00 mL。寫出酸性K2Cr2O7溶液滴定的離子方程式 ,則此錫粉樣品中錫的質量分數為__________________。
.2000 mol/L 酸性K2Cr2O7溶液滴定(產物中Cr呈+3價)至終點,消耗K2Cr2O7溶液15.00 mL。寫出酸性K2Cr2O7溶液滴定的離子方程式 ,則此錫粉樣品中錫的質量分數為__________________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省高一上半期考試化學卷(解析版) 題型:填空題
某一反應體系有反應物和生成物共五種物質:O2、H2CrO4、Cr(OH)3、H2O、 H2O2已知該反應中H2O2只發生如下過程:H2O2→O2
H2O2已知該反應中H2O2只發生如下過程:H2O2→O2
(1)該反應中的還原劑是 。
(2)該反應中,發生還原反應的過程是 (填氧化劑)→ 。(填還原產物)
(3)寫出該反應的化學方程式,并用單線橋法標出電子轉移的方向和數目:
(4)如反應轉移0.3mol電子,則產生的氣體在標準狀況下體積為 L。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省高一上半期考試化學卷(解析版) 題型:選擇題
NaBH4(其中H顯-1價)溶于水,并與水發生反應:NaBH4+2H2O = NaBO2+4H2↑下列關于該反應的說法正確的是()
A.NaBH4既是氧化劑,又是還原劑 B.NaBH4是氧化劑,H2O是還原劑
C.硼元素被氧化,氫元素被還原 D.氧化劑與還原劑的物質的量之比是2:1
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省高一上半期考試化學卷(解析版) 題型:選擇題
關于SO2的敘述中,正確的是( )
A.SO2的摩爾質量是64g B.1molSO2中所含分子數約為6.02×1023個
C.1 molSO2的質量是64g/mol D.常溫常壓下,1 molSO2的體積為22.4 L
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com