
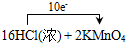 ═2KCl+2MnCl2+5Cl2↑+8H2O
═2KCl+2MnCl2+5Cl2↑+8H2O分析 (1)A.置換反應指一種單質與一種化合物反應生成另外一種單質與另外一種化合物;
B.氧化劑氧化性強于氧化產物氧化性;
C.反應②中還原劑為HCl,氧化劑為KMnO4,但起還原劑的作用的HCl占反應的HCl的$\frac{10}{16}$;
D.結合硫元素化合價變化計算轉移電子物質的量;
(2)反應中Mn元素化合價由+7價降低為+2,共轉移電子數為10,單線橋表示電子轉移時,在反應物中由失去電子的元素指向得電子元素,并注明轉移電子數目;
(3)①配制100mL0.5mol.L-1KMnO4溶液時需用的主要儀器有:托盤天平、藥匙、燒杯、玻璃棒、量筒、膠頭滴管、100mL容量瓶;
②根據n=cV計算KMnO4的物質的量,再根據m=nM計算其質量;
③分析操作對溶質物質的量、溶液體積的影響,再根據c=$\frac{n}{V}$分析對實驗結果的影響.
解答 解:(1)A.①③屬于置換反應,反應②不屬于置換反應,故A錯誤;
B.反應①中氧化劑為Cl2,氧化產物為Br2,氧化性Cl2>Br2,反應②中氧化劑為KMnO4,氧化產物為Cl2,氧化性KMnO4>Cl2,反應③中氧化劑為Br2,氧化產物為S,氧化性Br2>S,故氧化性:KMnO4>Cl2>Br2>S,故B正確;
C.反應②中還原劑為HCl,氧化劑為KMnO4,但起還原劑的作用的HCl占反應的HCl的$\frac{10}{16}$,還原劑與氧化劑的物質的量之比為16×$\frac{10}{16}$:2=5:1,故C錯誤;
D.反應硫元素化合價由-2價升高為0價,lmol還原劑(K2S)被氧化則轉移電子的物質的量為2mol,故D正確,
故選:BD;
(2)反應中Mn元素化合價由+7價降低為+2,共轉移電子數為10,用單線橋法標出反應電子轉移的方向和數目為: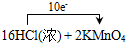 ═2KCl+2MnCl2+5Cl2↑+8H2O,
═2KCl+2MnCl2+5Cl2↑+8H2O,
故答案為: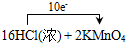 ═2KCl+2MnCl2+5Cl2↑+8H2O;
═2KCl+2MnCl2+5Cl2↑+8H2O;
(3)①配制100mL0.5mol.L-1KMnO4溶液時需用的主要儀器有:托盤天平、藥匙、燒杯、玻璃棒、量筒、膠頭滴管、100mL容量瓶,
故答案為:膠頭滴管、100mL容量瓶;
②KMnO4的物質的量為0.1L×0.5mol/L=0.05mol,其質量為0.05mol×158g/mol=7.9g,
故答案為:7.9;
③A.加水定容時俯視刻度線,液面在刻度線下方,溶液體積偏小,所配溶液濃度偏大,故A不符合;
B.需要加水定容,容量瓶內壁附有水珠而未干燥處理不影響所配溶液濃度,故B不符合;
C.顛倒搖勻后發現凹液面低于刻度線,少量溶液殘留在瓶口與瓶塞之間,又加水補上,溶液體積偏大,所配溶液濃度偏小,故C符合;
D.在溶解過程中有少量液體濺出燒杯外,移入容量瓶中溶質的物質的量偏小,所配溶液濃度偏小,故D符合,
故選:CD.
點評 本題考查氧化還原反應知識、一定物質的量濃度溶液配制,注意對基礎知識的理解掌握.


 輕巧奪冠周測月考直通中考系列答案
輕巧奪冠周測月考直通中考系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 新制氯水可使紫色石蕊試液先變紅后褪色 | |
| B. | 實驗室制取氯氣時,常用飽和石灰水來吸收多余的氯氣 | |
| C. | 漂白粉在漂白時產生次氯酸,所以漂白粉能使燃料等有機色素褪色 | |
| D. | 鉀元素顏色反應的操作是:將鉑絲放在稀鹽酸中洗滌后灼燒置無色,然后再用鉑絲蘸取固體氯化鉀,置于煤氣燈的火焰上進行灼燒,透過藍色鈷玻璃進行觀察 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 22.4L任何氣體的物質的量均為1mol | |
| B. | 非標準狀況下,1mol任何氣體不可能占有22.4L體積 | |
| C. | 0.4.molH2、0.2molO2、和0.4molCO2組成的混合氣體,在標準狀況下約為22.4L | |
| D. | 同溫、同壓下,相同質量的CO和CO2具有相同的體積 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4.6g金屬鈉與足量O2充分反應后,所得固體中陰、陽離子的總數為0.3NA | |
| B. | 1L 0.5 mol/L的FeCl3溶液充分水解后,所得Fe(OH)3膠粒的數目為0.5NA | |
| C. | 2.0g H218O與D2O的混合物中所含中子數為NA | |
| D. | 1L含NA個Al3+的Al(NO3)3液中,NO3-物質的量濃度大于3 mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. |  向容量瓶中轉移溶液 | B. |  中和熱的測定 | ||
| C. |  濃硫酸與銅的反應 | D. |  乙二酸晶體受熱分解 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1molAl3+離子含有的電子數為3NA | |
| B. | 1molCl2含有1 NA個原子 | |
| C. | 23g鈉在22.4L(標況下)Cl2中反應,轉移電子數NA個 | |
| D. | 欲配制1.00L 1.00mol.L-1的NaCl溶液,可將 58.5gNaCl溶于 1.00L水中 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com