
分析 (1)濃硫酸具有強氧化性,它可把不活潑的金屬銅氧化.氧化還原反應中化合價升高,失電子做還原劑被氧化,發生氧化反應,其產物為氧化產物;化合價降低,得到電子做氧化劑,被還原,發生還原反應;
(2)反應中Cu的化合價從0價升高到-2價,結合方程式計算;
(3)氧化還原反應中還原劑的還原性大于還原產物.
解答 解:(1)濃硫酸具有強氧化性,它可把不活潑的金屬銅氧化.反應中濃硫酸中S的化合價降低,濃硫酸作氧化劑,Cu失電子做還原劑被氧化,其產物CuSO4為氧化產物;
故答案為:氧化;氧化;CuSO4;
(2)反應中Cu的化合價從0價升高到-2價,消耗了32g Cu,即$\frac{32g}{64g/mol}$=0.5mol,則轉移電子為1mol,由Cu+2H2SO4(濃)?CuSO4+SO2↑+2H2O可知,還原了0.5mol硫酸,生成0.5mol二氧化硫,即11.2L;
故答案為:1;0.5;11.2;
(3)氧化還原反應中還原劑的還原性大于還原產物,反應中Cu作還原劑,SO2作還原產物,則還原性:Cu>SO2,故答案為:>.
點評 本題考查了氧化還原反應的概念判斷,主要是氧化還原反應的特征應用,化合價的變化判斷是解題關鍵,題目難度不大.


 金牌教輔培優優選卷期末沖刺100分系列答案
金牌教輔培優優選卷期末沖刺100分系列答案科目:高中化學 來源: 題型:選擇題
| A. | 1種 | B. | 3種 | C. | 5種 | D. | 7種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鈉與水反應:Na+H2O=Na++OH-+H2↑ | |
| B. | 鋁與鹽酸反應:2Al+6H+=2Al3++3H2↑ | |
| C. | 氫氧化鋁與鹽酸反應:OH-+H+=H2O | |
| D. | 氯化鋁與氨水反應:Al3++3OH-=Al(OH)3↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
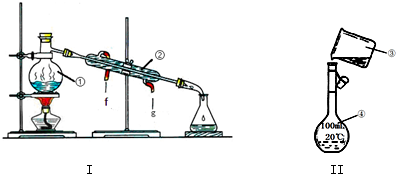
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


 .E中含氧官能團的名稱為醛基和羥基.
.E中含氧官能團的名稱為醛基和羥基. .寫出有關反應的類型:②氧化反應⑥消去反應.
.寫出有關反應的類型:②氧化反應⑥消去反應.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
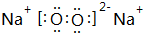 ,寫出M2Z2與水反應的離子方程式:2Na2O2+2H2O=4Na++4OH-+O2↑.
,寫出M2Z2與水反應的離子方程式:2Na2O2+2H2O=4Na++4OH-+O2↑.查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com