
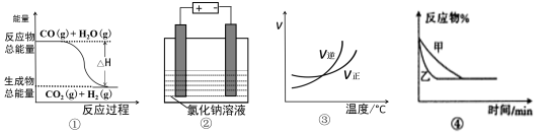
| A. | 圖①表示可逆反應(yīng):CO(g)+H2O(g)?CO2(g)+H2(g)△H<0 | |
| B. | 圖②表示用惰性電極電解足量氯化鈉溶液.一段時間后,兩極上可收集到相等體積的氣體 | |
| C. | 圖③表示可逆反應(yīng):A2(g)+3B2(g)?2AB3(g)△H<0 | |
| D. | 圖④表示壓強對可逆反應(yīng)2A(g)+B(g)?3C(g)+D(s)的影響,乙壓強大 |
分析 A.由圖可知,CO(g)、H2O(g)的總能量比CO2(g)、H2(g)的總能量高;
B.惰性電極解足量的氯化鈉溶液,發(fā)生2NaCl+2H2O$\frac{\underline{\;電解\;}}{\;}$2NaOH+H2↑+Cl2↑;
C.由圖可知,交叉點后升高溫度,逆反應(yīng)速率大于正反應(yīng)速率,可知升高溫度平衡逆向移動;
D.2A(g)+B(g)?3C(g)+D(s)為反應(yīng)前后體積不變的反應(yīng),則增大壓強,反應(yīng)速率加快,平衡不移動.
解答 解:A.圖①反應(yīng)物總能量大于生成物總能量,反應(yīng)放熱,則CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,故A正確;
B.圖②電解足量氯化鈉溶液,陽極生成Cl2,陰極生成H2,物質(zhì)的量相同,但體積受溫度、壓強影響,且氯氣與水反應(yīng),則陰、陽極產(chǎn)生氣體體積不相等,故B錯誤;
C.圖③隨著溫度的升高,逆反應(yīng)速率大于正反應(yīng)速率,平衡向逆方向進行,說明反應(yīng)放熱,則A2(g)+3B2(g)?2AB3(g)△H<0,故C正確;
D.圖④中因乙先到達平衡,故乙的壓強大,甲的壓強小,但增大壓強,平衡向正反應(yīng)方向移動,反應(yīng)物百分含量減少與圖象相符,故D正確.
故選B.
點評 本題考查化學平衡的影響因素及反應(yīng)熱、焓變,為高頻考點,把握圖中能量變化、壓強對平衡移動的影響為解答的關(guān)鍵,側(cè)重分析與應(yīng)用能力的考查,注意選項B為解答的難點,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | H2SO4→H2++SO42- | B. | NH3•H2O?NH4++OH- | ||
| C. | Ca(OH)2?Ca2++2OH- | D. | NaHCO3→Na++H++CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 維生素C和脫氫維生素C | B. | 維生素C和HI | ||
| C. | I2和HI | D. | I2和脫氫維生素C |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 36 | B. | 24 | C. | 20 | D. | 10 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用聚氯乙烯樹脂生產(chǎn)食品包裝袋 | |
| B. | 用工業(yè)酒精勾兌白酒 | |
| C. | 合理利用可燃冰有利于彌補能源短缺 | |
| D. | 用含甲酚的藥皂除菌消毒,是利用酚類物質(zhì)的強氧化性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 空氣電極是負極 | |
| B. | 電子由鋁合金電極經(jīng)電解質(zhì)溶液流向空氣電極 | |
| C. | 負極的反應(yīng)式為:O2+2 H2O+4 e-=4 OH- | |
| D. | 電池工作時鋁合金電極不斷被消耗 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO2和濕潤的Cl2都有漂白性,推出二者混合后漂白性更強 | |
| B. | 根據(jù)溶液的pH與溶液酸堿性的關(guān)系,推出pH=7.0的溶液一定顯中性 | |
| C. | 根據(jù)F、Cl、Br、I非金屬性依次減弱,推出HF、HC1、HBr、HI的還原性依次增強 | |
| D. | 結(jié)構(gòu)和組成相似的物質(zhì),沸點隨相對分子質(zhì)量增大而升高,因此NH3沸點低于PH3 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com