
| A. | 5.6g鐵粉與氯氣充分反應失去的電子數一定為0.3NA | |
| B. | 0.1mol Zn與含0.1mol HCl的鹽酸充分反應,轉移的電子數目為0.2NA | |
| C. | 1mol Na與足量O2反應,生成Na2O和Na2O2的混合物,轉移的電子數為NA | |
| D. | 向FeCl2溶液中通入Cl2,當有1molFe2+被氧化時,共轉移的電子的數目為NA |
分析 A、依據n=$\frac{m}{M}$計算物質的量,結合鐵和氯氣反應生成氯化鐵分析;
B、0.1molZn與含0.1molHCl的鹽酸溶液反應時,鋅過量,鹽酸完全反應;
C、依據1molNa參與反應失去1mol電子分析;
D、依據當有1molFe2+被氧化生成三價鐵時失去1mol電子分析;
解答 解:A、5.6g鐵粉物質的量為0.1mol,與氯氣反應生成氯化鐵,失去的電子數為0.3NA,故A正確;
B、0.1molZn與含0.1molHCl的鹽酸溶液反應時,鋅過量,鹽酸完全反應,故轉移的電子的物質的量由鹽酸決定,故0.1mol鹽酸轉移0.1mol電子,故B錯誤;
C、因為鈉被氧化生成+1價的鈉離子,所以1molNa參與反應失去1mol電子,則1mol Na與足量O2反應,生成Na2O和Na2O2的混合物,轉移的電子數為NA,故C正確;
D、因為有1molFe2+被氧化生成三價鐵時失去1mol電子,所以向FeCl2溶液中通入Cl2,當有1molFe2+被氧化時,共轉移的電子的數目為NA,故D正確;
故選B.
點評 本題考查了阿伏伽德羅常數的分析判斷,主要是氧化還原反應轉移電子數的計算,題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2O2 Na2O | B. | KClO NaOH | C. | Br2 HBr | D. | HF H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
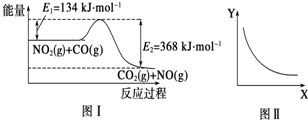
| A. | 一定條件下,向密閉容器中加入1 mol NO2(g)與1 mol CO(g)放出234 kJ熱量 | |
| B. | 若X表示CO的起始濃度,則Y表示的可能是NO2的轉化率 | |
| C. | 若X表示溫度,則Y表示的可能是CO2的物質的量濃度 | |
| D. | 若X表示反應時間,則Y表示的可能是混合氣體的密度 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CuSO4 | B. | Ca(NO3)2 | C. | Na2CO3 | D. | FeCl3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該化合物可能為2甲基2丙醇 | B. | 該化合物為2丁醇的同分異構體 | ||
| C. | 該化合物可能為乙醚 | D. | 該化合物為乙醚的同系物 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com