
用溶質質量分數為98%的濃硫酸和溶質質量分數為18%的稀硫酸配制500 g溶質質量分數為28%的硫酸,需要濃硫酸和稀硫酸的質量分別為( )
A.62.5 g 437.5 g B.71.4 g 428.6 g
C.437.5 g 62.5 g D.428.6 g 71.4 g
 名師點撥卷系列答案
名師點撥卷系列答案 英才計劃期末調研系列答案
英才計劃期末調研系列答案科目:高中化學 來源: 題型:
設NA表示阿伏加德羅常數的值。下列說法正確的是( )
A.標準狀況下,0.1 mol Cl2溶于水,轉移的電子數目為0.1NA
B.常溫常壓下,18 g H2O中含有的原子總數為3NA
C.標準狀況下,11.2 L CH3CH2OH中含有的分子數目為0.5NA
D.常溫常壓下,2.24 L CO和CO2混合氣體中含有的碳原子數目為0.1NA
查看答案和解析>>
科目:高中化學 來源: 題型:
NA代表阿伏加德羅常數的數值,下列說法正確的是( )
A.1 mol Cl2參加的任何反應轉移電子數都是2NA
B.標準狀況下,22.4 mL水中含有的分子數目約為1.24NA
C.常溫常壓下,29 g乙基(—C2H5)所含電子數為13NA
D.0.2 mol Na2O2中含有離子總數為0.6NA
查看答案和解析>>
科目:高中化學 來源: 題型:
在標準狀況下,將V L A氣體(摩爾質量為M g·mol-1)溶于0.1 L水中,所得溶液的密度為ρ g·cm-3,則此溶液的物質的量濃度(mol·L-1)為( )
A.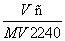 B.
B.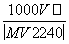
C.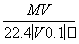 D.1 000VρM(MV+2 240)
D.1 000VρM(MV+2 240)
查看答案和解析>>
科目:高中化學 來源: 題型:
正誤判斷,正確的劃“√”,錯誤的劃“×”
(1)使用托盤天平稱量藥品,都不能直接放在托盤中,均應放兩張相同的紙片( )
(2)定容時,往容量瓶中緩慢加蒸餾水,等液面離容量瓶刻度線1~2 mL時,改用膠頭滴管滴加蒸餾水( )
查看答案和解析>>
科目:高中化學 來源: 題型:
正誤判斷,正確的劃“√”,錯誤的劃“×”
(1)用容量瓶配溶液時,若加水超過刻度線,立即用滴管吸出多余液體( )
(2014·新課標全國卷Ⅰ,12D)
(2)配制溶液定容時,俯視容量瓶刻度會使溶液濃度偏高( )
(2014·大綱全國卷,6C)
(3)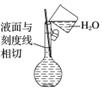 配制溶液( )
配制溶液( )
(2014·山東理綜,10A)
(4)因為KNO3的溶解度大,所以可用重結晶法除去KNO3中混有的NaCl( )
(2014·廣東理綜,9A)
(5)因為Ca(OH)2能制成澄清石灰水,所以可配制2.0 mol·L-1的Ca(OH)2溶液( )
(2014·廣東理綜,9D)
(6)配制0.100 0 mol·L-1氯化鈉溶液時,將液體轉移到容量瓶中需用玻璃棒引流( )
(2013·福建理綜,10C)
(7)用容量瓶配制溶液,定容時俯視刻度線,所配溶液濃度偏小( )
(2013·天津理綜,4B)
(8)用固體NaCl配制0.5 mol·L-1的溶液,所用的儀器有:燒杯、玻璃棒、膠頭滴管、容量瓶( )
(2013·山東理綜,11C)
(9)用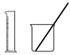 配制100 mL 0.100 0 mol·L-1 K2Cr2O7溶液( )
配制100 mL 0.100 0 mol·L-1 K2Cr2O7溶液( )
(2012·天津理綜,4D)
(10)在50 mL量筒中配制0.100 0 mol·L-1碳酸鈉溶液( )
(2012·福建理綜,6C)
(11)用100 mL容量瓶、燒杯、玻璃棒、膠頭滴管和pH=1的鹽酸配制100 mL pH=2的鹽酸( )
(2012·安徽理綜,10B改編)
(12)用量筒量取20 mL 0.500 0 mol·L-1 H2SO4溶液于燒杯中,加水80 mL,配制成0.100 0 mol·L-1 H2SO4溶液( )
(2011·江蘇,7B)
(13)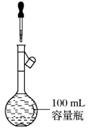 定容操作( )
定容操作( )
(2010·安徽理綜,8B)
(14)配制溶液時,若加水超過容量瓶刻度,應用膠頭滴管將多余溶液吸出( )
(2010·山東理綜,14B)
查看答案和解析>>
科目:高中化學 來源: 題型:
下列關于晶體的說法一定正確的是( )
A.分子晶體中都存在共價鍵
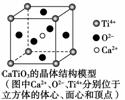
B.CaTiO3晶體中每個Ti4+和12個O2-相緊鄰
C.SiO2晶體中每個硅原子與兩個氧原子以共價鍵相結合
D.金屬晶體的熔點都比分子晶體的熔點高
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com