
| A. | CaCO3(固) | B. | NaCl溶液 | C. | KNO3溶液 | D. | CuSO4(固) |
分析 為了減緩反應速率且不影響生成H2的總量,可使溶液中H+濃度降低,但總量不變,以此解答該題.
解答 解:A.加入CaCO3固體,消耗H+,生成氫氣的總量較少,故A錯誤;
B.加入NaCl溶液,H+濃度降低,但總量不變,可減緩反應速率且不影響生成H2的總量,故B正確;
C.加入KNO3溶液,生成NO氣體,不生成氫氣,故C錯誤;
D.加入CuSO4固體,置換出銅,形成原電池反應,反應速率加快,故D錯誤.
故選B.
點評 本題考查化學反應速率的影響因素,為高考高頻考點,側重于基本概念的綜合考查和運用,難度大不,注意把握題目要求以及影響反應速率的因素,學習中要注意相關基礎知識的學習和積累.


 舉一反三期末百分沖刺卷系列答案
舉一反三期末百分沖刺卷系列答案科目:高中化學 來源: 題型:選擇題
 近年來,科學家合成了一種穩定的氫鋁化合物Al2H6.Al2H6的球棍模型如圖所示,它的熔點為150℃,可用作高能燃料或儲氫材料.下列說法正確的是( )
近年來,科學家合成了一種穩定的氫鋁化合物Al2H6.Al2H6的球棍模型如圖所示,它的熔點為150℃,可用作高能燃料或儲氫材料.下列說法正確的是( )| A. | 1molAl2H6中約含有4.8×1024個σ鍵 | |
| B. | 60gAl2H6中含鋁原子約為1.2×1023個 | |
| C. | Al2H6可以燃燒,產物為氧化鋁和水 | |
| D. | Al2H6在固態時所形成的晶體是離子晶體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
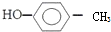
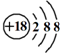
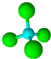
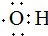
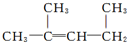 的名稱:1,3-二甲基-2丁烯( )
的名稱:1,3-二甲基-2丁烯( )| A. | ⑤ | B. | ④⑤ | C. | ③⑦ | D. | ②⑧ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
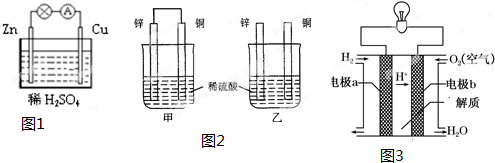
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4L CCl4含有的分子數為NA | |
| B. | 常溫常壓下,17g NH3所含的原子數目為4NA | |
| C. | 鋁與足量鹽酸反應,生成2.24L H2時,轉移的電子數為0.2NA | |
| D. | 0.1mol/L Na2CO3溶液中含有的Na+數目為0.2NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com