
| 溫度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常數 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
| c(C)?c(D) |
| c(A)?c(B) |
| c(C)?c(D) |
| c(A)?c(B) |
| 0.2mol |
| 5L |
| x?x |
| (0.04-x)×(0.16-x) |
| 0.032mol/L |
| 0.04mol/L |


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化學 來源: 題型:
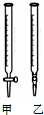 某學生用0.1000mol?L-1標準NaOH溶液滴定未知濃度的鹽酸,其操作可分解為以下幾步:
某學生用0.1000mol?L-1標準NaOH溶液滴定未知濃度的鹽酸,其操作可分解為以下幾步:| 滴定次數 | 待測溶液的體積(/mL) | 標準NaOH溶液的體積 | |
| 滴定前讀數(/mL) | 滴定后讀數(/mL) | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、不慎將濃硫酸沾到皮膚上,立即用水沖洗,再涂上3%-5%的NaHCO3溶液 |
| B、濃堿沾到皮膚上,立即用大量的水沖洗,再涂上3%-5%的硼酸溶液 |
| C、酒精著火,應移開可燃物,用濕布或沙土蓋滅 |
| D、將煤氣中毒者轉移到通風處搶救 |
查看答案和解析>>
科目:高中化學 來源: 題型:
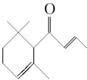 ,有關該化合物的下列說法不正確的是( )
,有關該化合物的下列說法不正確的是( )| A、分子式為C13H20O |
| B、該化合物可發生銀鏡反應 |
| C、該物質不屬于醇類 |
| D、與溴的CCl4溶液反應生成的產物經水解、稀硝酸酸化后可用AgNO3溶液檢驗. |
查看答案和解析>>
科目:高中化學 來源: 題型:
| ①稀鹽酸溶液 |
| ②50mL0.11mol/的過量草酸銨溶 |
| ③過濾 |
| ④加酸溶液 |
| ⑤用標準高錳 |
| 酸鉀溶液滴定 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 用如圖裝置電解硫酸鉀溶液來制取氧氣、氫氣、硫酸和氫氧化鉀.
用如圖裝置電解硫酸鉀溶液來制取氧氣、氫氣、硫酸和氫氧化鉀.查看答案和解析>>
科目:高中化學 來源: 題型:
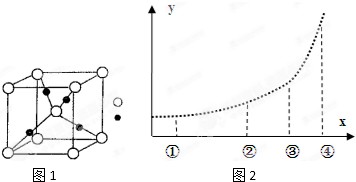
查看答案和解析>>
科目:高中化學 來源: 題型:
| 有機物 | 乙烯 | 乙炔 | 環己烷 | 苯 |
| Ω | 1 | 2 | 1 | 4 |
| A、1molΩ=3的不飽和鏈烴再結合6molH 即達到飽和 |
| B、C10H8的Ω=7 |
| C、C4H8的不飽和度與C3H6、C2H4的不飽和度不相同 |
| D、CH3CH=CHCH3與環丁烷的不飽和度相同 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com