
在10L恒容密閉容器中充入X(g)和Y(g),發(fā)生反應X(g)+Y(g) M(g)+N(g),所得實驗數據如下表:
M(g)+N(g),所得實驗數據如下表:
| 實驗 編號 | 溫度/℃ | 起始時物質的量/mol | 平衡時物質的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| ④ | 900 | 0.10 | 0.15 | b |
C
解析試題分析:A、實驗①中,若5min時測得n(M)=0.050mol,濃度是0.0050mol/L,則根據反應的化學方程式可知,同時生成的N的物質的量也是0.0050mol/L ,因此0至5min時間內,用N表示的平均反應速率υ(N)=0.0050mol/L ÷5min=1.0×10-3mol/(L·min),A不正確;B、實驗②中,平衡時M的濃度是0.0080mol/L,則同時生成的N的濃度是0.0080mol/L,消耗X與Y的濃度均是0.0080mol/L,因此平衡時X和Y的濃度分別為0.01mol/L-0.0080mol/L=0.002mol/L,0.04mol/L-0.0080mol/L=0.032mol/L,因此反應的平衡常數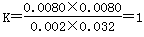 ,B不正確;C、根據反應的化學方程式可知,如果X的轉化率為60%,則
,B不正確;C、根據反應的化學方程式可知,如果X的轉化率為60%,則
X(g) + Y(g) M(g) + N(g)
M(g) + N(g)
起始濃度(mol/L) 0.020 0.030 0 0
轉化濃度(mol/L) 0.012 0.012 0.012 0.012
平衡濃度(mol/L)0.008 0.018 0.012 0.012
溫度不變,平衡常數不變,則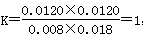 ,即反應達到平衡狀態(tài),因此最終平衡時X的轉化率為60%。C正確;D、700℃時
,即反應達到平衡狀態(tài),因此最終平衡時X的轉化率為60%。C正確;D、700℃時
X(g) + Y(g) M(g) + N(g)
M(g) + N(g)
起始濃度(mol/L) 0.040 0.010 0 0
轉化濃度(mol/L) 0.009 0.009 0.009 0.009
平衡濃度(mol/L)0.031 0.001 0.009 0.009
則該溫度下平衡常數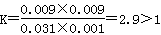 ,這說明升高溫度平衡常數減小,即平衡向逆反應方向移動,因此正方應是放熱反應。若容器④中溫度也是800℃,由于反應前后體積不變,則與③相比④平衡是等效的,因此最終平衡時M的物質的量b=0.5a=0.06。當溫度升高到900℃時平衡顯逆反應方向移動,因此b<0.060,D不正確,答案選C。
,這說明升高溫度平衡常數減小,即平衡向逆反應方向移動,因此正方應是放熱反應。若容器④中溫度也是800℃,由于反應前后體積不變,則與③相比④平衡是等效的,因此最終平衡時M的物質的量b=0.5a=0.06。當溫度升高到900℃時平衡顯逆反應方向移動,因此b<0.060,D不正確,答案選C。
考點:考查化學反應速率和化學平衡常數的有關判斷與計算


 培優(yōu)好卷單元加期末卷系列答案
培優(yōu)好卷單元加期末卷系列答案 一線名師權威作業(yè)本系列答案
一線名師權威作業(yè)本系列答案科目:高中化學 來源: 題型:單選題
在一密閉容器中,反應aA(g) bB(g)達平衡后,保持溫度不變,將容器容積增加一倍,達到新平衡時,B的濃度是原來的60%。則下列敘述正確的是( )
bB(g)達平衡后,保持溫度不變,將容器容積增加一倍,達到新平衡時,B的濃度是原來的60%。則下列敘述正確的是( )
| A.a>b | B.平衡向正反應方向移動 |
| C.A的轉化率減小 | D.B的質量分數減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
一定溫度下,在2L的密閉容器中發(fā)生如下反應: B、C的物質的量隨時間變化的關系如圖l,達平衡后在
B、C的物質的量隨時間變化的關系如圖l,達平衡后在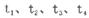 時都只改變了一種條件,逆反應速率隨時間變化的關系如圖2。下列有關說法正確的是
時都只改變了一種條件,逆反應速率隨時間變化的關系如圖2。下列有關說法正確的是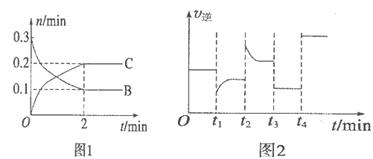
A.x=2,反應開始2 min內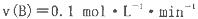
B.t1時是降溫,平衡逆向移動
C.t2時改變的條件可能是增大c(C),平衡時B的物質的量分數增大
D.t3時可能是減小壓強,平衡不移動;t4時可能是使用催化劑,c (B)不變
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在體積一定的密閉容器中發(fā)生反應:2NH3(g) N2(g)+3H2(g),在673K、30MPa下,n(NH3)和n(N2)隨時間變化的關系如圖所示。下列敘述正確的是
N2(g)+3H2(g),在673K、30MPa下,n(NH3)和n(N2)隨時間變化的關系如圖所示。下列敘述正確的是 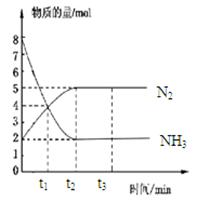
| A.t1時反應達到平衡 |
| B.t3時,v正(N2)﹥v逆(N2) |
| C.t2時和t3時n(H2)相等 |
| D.t3后,若體積不變充He,反應速率增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在一定條件下,N2O分解的部分實驗數據如下:
下圖能正確表示該反應有關物理量變化規(guī)律的是
(注:圖中半衰期指任一濃度N2O消耗一半時所需的相應時間,c1、c2均表示N2O初始濃度且c1<c2)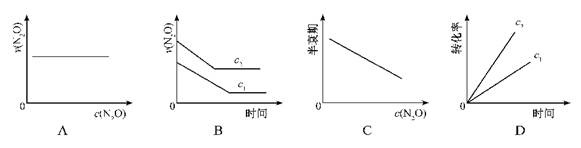 、
、
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
己知: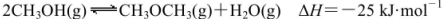 。某溫度下的平衡常數為400。此溫度下,在1L體積不變的密閉容器中加入CH3OH,某時刻測得各組分的物質的量濃度如表,下列說法中不正確的是
。某溫度下的平衡常數為400。此溫度下,在1L體積不變的密閉容器中加入CH3OH,某時刻測得各組分的物質的量濃度如表,下列說法中不正確的是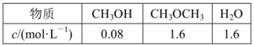
| A.此時刻反應達到平衡狀態(tài) |
| B.容器內壓強不變時,說明反應達平衡狀態(tài) |
| C.平衡時,再加入與起始等量的CH3OH,達新平衡后CH3OH轉化率不變 |
| D.平衡時,反應混合物的總能量降低40 kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
向一容積為1L的密閉容器中加入一定量的X、Y,發(fā)生化學反應aX(g)+2Y(s)  bZ(g) △H<0。下圖是容器中X、Z的物質的量濃度隨時間變化的曲線。
bZ(g) △H<0。下圖是容器中X、Z的物質的量濃度隨時間變化的曲線。
根據以上信息判斷,下列說法中正確的是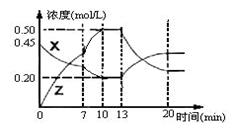
| A.用X表示0~10min內該反應的平均速率為v(X)=0.045mol/(L·min) |
| B.化學方程式中a:b= 1:3, |
| C.推測在第7min時曲線變化的原因可能是增加X的濃度 |
| D.推測該反應處于化學平衡狀態(tài)的時間是10min--13min及第20min 后 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
一定條件下,將A、B、C三種物質各1 mol通入一個密閉容器中發(fā)生反應:2A+B 2C,達到化學反應限度時,B的物質的量可能是( )
2C,達到化學反應限度時,B的物質的量可能是( )
A.1.5 mol B.1 mol C.0.5 mol D.0
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
可逆反應:2SO2(g)+O2(g) 2SO3(g)在一個體積不變的密閉容器中反應,達到平衡狀態(tài)的標志是( )
2SO3(g)在一個體積不變的密閉容器中反應,達到平衡狀態(tài)的標志是( )
①單位時間內消耗n mol SO2的同時,生成n mol SO2
②單位時間內消耗2n mol SO2的同時,生成n mol O2
③用SO2、O2、SO3的物質的量濃度變化表示的反應速率的比為2︰1︰2的狀態(tài)
④混合氣體的密度不再改變的狀態(tài)
| A.①② | B.①②④ | C.①③④ | D.②③④ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com