
恒溫恒容下,向2 L密閉容器中加入MgSO4(s)和CO(g),發生反應:
MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g)
MgO(s)+CO2(g)+SO2(g)
反應過程中測定的部分數據見下表:
反應時間/min | n(MgSO4)/mol | n(CO)/mol | n(SO2) / mol |
0 | 2.0 | 2.0 | 0 |
2 | 0.8 | ||
4 | 1.2 | ||
6 | 1.2 | 2.8 |
下列說法正確的是
A.0~2 min內的平均速率為υ (CO)=0.6 mol/(L·min)
B.4 min后,平衡移動的原因可能是向容器中加入了2.0 mol的SO2
C.4 min后,若升高溫度,SO2物質的量濃度變為0.7mol/L,則正反應為放熱反應
D.其他條件不變,若起始時容器中MgSO4、CO均為1.0 mol,則平衡時n(SO2)=0.6 mol
科目:高中化學 來源:2016屆貴州省興義市高三上學期期中測試理綜化學試卷(解析版) 題型:選擇題
下列離子方程式正確的是:
A.過量氯氣通入溴化亞鐵溶液中:Fe2++2Br-+2Cl2=Fe3++Br2+4Cl-
B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O
C.碳酸氫鈣和過量的氫氧化鈉溶液反應:Ca2++ OH—+HCO3—=CaCO3↓+ H2O
D.用FeCl3溶液腐蝕印刷電路板:Cu+Fe3+=Fe2++Cu2+
查看答案和解析>>
科目:高中化學 來源:2016屆河北省邯鄲市高三上學期10月月考化學試卷(解析版) 題型:填空題
下圖為元素周期表的一部分,請參照元素①~⑧在表中的位置,回答下列問題:

(1)表中某元素最高正價氧化物的水化物與其氫化物之間能相互反應生成離子化合物,則該離子化合物的名稱是______,由元素④、⑥、⑦、⑧形成的簡單離子的半徑由大到小的順序是_______(用離子符號表示,下同)。②、④、⑤元素的氫化物的沸點由高到低的順序是____________。
(2)分別由上述兩種元素組成、均為10e-的陰、陽離子,在加熱條件下反應生成兩種10e-的分子,寫出該離子反應方程是________________。
(3)由表中四種元素形成X、Y、Z、M、N等常見物質,X、Y含有一種相同元素,其中X焰色反應呈黃色,可發生以下反應:
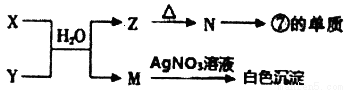
① X、Y與水混合后反應的離子方程式為________________。
② N→⑦的單質反應的化學方程式為_________________。
③ 元素④形成的單質的電子式為________________。
查看答案和解析>>
科目:高中化學 來源:2016屆安徽省高三上學期開學聯考化學試卷(解析版) 題型:實驗題
三草酸合鐵酸鉀晶體K3[Fe(C2O4)3]?3H2O可用于攝影和藍色印刷.某小組將無水三草酸合鐵酸鉀在一定條件下加熱分解,對所得氣體產物和固體產物進行實驗和探究.請利用實驗室常用儀器、用品和以下限選試劑完成驗證和探究過程.
限選試劑:濃硫酸、1.0mol•L﹣1HNO3、1.0mol•L﹣1鹽酸、1.0mol•L﹣1NaOH、3%H2O2、0.1mol•L﹣1KI、0.1mol•L﹣1CuSO4、20%KSCN、澄清石灰水、氧化銅、蒸餾水.
(1)該小組同學查閱資料后推知,固體產物中,鐵元素不可能以三價形式存在,而鹽只有K2CO3.通過 可驗證固體產物中是否含有鉀元素.
(2)固體產物中鐵元素存在形式的探究.
①提出合理假設:
假設1:全部是鐵單質;
假設2: ;
假設3: .
②設計實驗方案證明你的假設
③實驗過程
根據②中方案進行實驗.在寫出實驗步驟、預期現象與結論.

查看答案和解析>>
科目:高中化學 來源:2016屆福建省四地六校高三上學期第一次聯考化學試卷(解析版) 題型:選擇題
碘是一種與人的生命活動密切相關的元素,已知I2能溶于NaOH或KI溶液,反應方程式分別為:3I2+6OH﹣═5I﹣+IO3-+3H2O(HIO不穩定,易發生歧化反應)和I2+I﹣═I3-,溴化碘(IBr)是一種鹵素互化物,具有與鹵素單質相似的性質,下列反應方程式中不正確的是
A.IBr加入Na2S溶液中產生黃色渾濁:IBr+S2﹣═I﹣+Br﹣+S↓
B.IBr加入KI溶液中:IBr+2I﹣═Br﹣+ I3-
C.IBr加入NaOH溶液中:IBr+2OH﹣═BrO﹣+I﹣+H2O
D.IBr加入AgNO3溶液中:3IBr+5Ag++3H2O═3AgBr↓+2AgI↓+ IO3-+6H+
查看答案和解析>>
科目:高中化學 來源:2016屆江西省吉安市高三上學期第一次月考化學試卷(解析版) 題型:選擇題
NA為阿伏加德羅常數的值 下列說法正確的是
A.現有乙烯、丙烯、丁烯的混合氣體共14g,其原子數為3NA
B.標準狀況下,11.2L的戊烷所含的分子數為0.5NA
C.標準狀況下,2.24 L Cl2溶于水中達到飽和,轉移的電子數是0.1NA
D.25℃時,pH=13的1.0L Ba(OH)2溶液中含有的OH﹣數目為0.2NA
查看答案和解析>>
科目:高中化學 來源:2015-2016學年陜西省西安市高一上10月月考化學試卷(解析版) 題型:填空題
(18分)(1)標準狀況下,67.2L CO2約是___________ mol,約含有___________個CO2 分子,其中約含有___________ mol氧原子。
(2)要得到含溶質0.2mol的溶液,需取0.05mol/L的氫氧化鋇溶液___________mL。
(3)9.2g氮的氧化物NOx中含有N原子數為0.2mol,則NOx的摩爾質量為__________,x的數值為___________,這些質量的NOx在標準狀況下的體積約為_____________L。
(4)常溫下,相對分子質量為M的某無水鹽A的溶解度為Sg,則常溫時,該鹽飽和溶液質量分數為__________,如果已知該飽和溶液的密度為ρg/cm3,則該溶液的物質的量濃度為___________。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山西省高一上期中考試化學試卷(解析版) 題型:填空題
(6分)I. (1)在Al2(SO4)3和MgSO4組成的混合物中,Al3+與Mg2+的物質的量之比為2∶3,則在含有4 mol SO42-的混合物中,MgSO4的質量是______________克。
(2)V ml Al2(SO4)3溶液中含有Al3+ a g,取V/4 ml溶液稀釋到4V ml,則稀釋后溶液中SO42-的物質的量濃度是______________ mol/L。
II.在120 ℃時分別進行如下四個反應:
A.2H2S (g) + O2 (g) ==2H2O (g)+2S (s) B.2H2S (g)+3O2 (g)==2H2O (g)+2SO2 (g)
C.C2H4 (g)+3O2 (g)==2H2O (g)+2CO2 (g) D.C4H8 (g)+6O2 (g)==4H2O (g)+4CO2 (g)
(1)若反應在容積固定的容器內進行,反應前后氣體密度(d)和氣體總壓強(p)分別符合關系式d前=d后和p前>p后的是__________;符合關系式d前=d后和p前=p后的是__________。(請填寫反應的代號)
(2)若反應在壓強恒定容積可變的容器內進行,反應前后氣體密度(d)和氣體體積(V)分別符合關系式d前>d后和V前<V后的是________;符合d前>d后和V前>V后的是________。(請填寫反應的代號)
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河南信陽高級中學高二開學考試化學試卷(解析版) 題型:選擇題
下列大小比較正確的是
A.穩定性:HI>HBr>HCl>HF B.元素非金屬性:Si>P>S>Cl
C.沸點: 正丁烷>異丁烷>丙烷 D.堿性NaOH>KOH>Ca(OH)2>Ba(OH)2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com