
| 酸或堿 | 電離平衡常數(Ka或Kb) |
| CH3COOH | 1.7×10-5mol?L-1 |
| HNO2 | 7.1×10-4mol?L-1 |
| HCN | 6.2×10-10mol?L-1 |
| HClO | 4.7×10-8mol?L-1 |
| NH3?H2O | 1.7×10-5mol?L-1 |


科目:高中化學 來源: 題型:
| A、摩爾是國際單位制中的七個物理量之一 |
| B、摩爾是物質的量的單位,簡稱摩,符號為mol |
| C、氧氣的摩爾質量為32g |
| D、每摩爾任何物質均含有6.02×1023個原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:
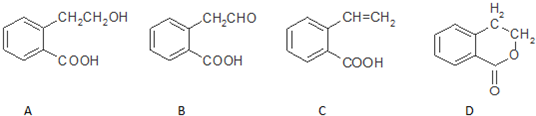
查看答案和解析>>
科目:高中化學 來源: 題型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 (1)硼酸(H3BO3)溶液中存在如下平衡:
(1)硼酸(H3BO3)溶液中存在如下平衡:| 化學式 | H2CO3 | CH3COOH |
| 電離常數 | K1=4.4×10-7 K2=4.7×10-11 | K=1.75×10-5 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 主 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ? | ? |
查看答案和解析>>
科目:高中化學 來源: 題型:
 A、B、C三種短周期元素在周期表中相對位置如表格:
A、B、C三種短周期元素在周期表中相對位置如表格:| A | |||
| B | C |
查看答案和解析>>
科目:高中化學 來源: 題型:
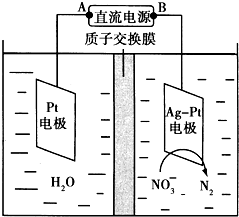 化學在環境保護中起著十分重要的作用.催化反硝化法和電化學降解法可用于治理水中硝酸鹽的污染.
化學在環境保護中起著十分重要的作用.催化反硝化法和電化學降解法可用于治理水中硝酸鹽的污染.
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、密度比為11:16 |
| B、物質的量比為16:11 |
| C、體積比為11:16 |
| D、分子個數比為16:11 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com