
| c(OH-) |
| c(H+) |
| c(OH-) |
| c(H+) |
| 1.8×10-11 |
| 8.1×10-9 | ||
|
| 8.1×10-9 | ||
|
| 1.8×10-11 |


 星級口算天天練系列答案
星級口算天天練系列答案 芒果教輔達標測試卷系列答案
芒果教輔達標測試卷系列答案科目:高中化學 來源: 題型:
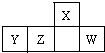 短周期元素X、Y、Z、W在周期表中的相對位置如圖,W原子的最外層電子數是其最內層電子數的3倍.下列判斷正確的是( )
短周期元素X、Y、Z、W在周期表中的相對位置如圖,W原子的最外層電子數是其最內層電子數的3倍.下列判斷正確的是( )| A、原子半徑:X>Y>Z>W |
| B、Y、Z是金屬元素 |
| C、最簡單氣態氫化物的熱穩定性:Z>W |
| D、X的氫化物能與其最高價氧化物對應的水化物反應生成鹽 |
查看答案和解析>>
科目:高中化學 來源: 題型:
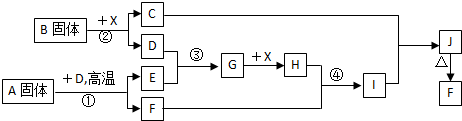
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、用醋酸除去暖瓶中的水垢:2H++CaCO3═Ca2++CO2↑+H2O |
| B、利用Na2CO3溶液可除油污:CO32-+2H2O?H2CO3+2OH- |
| C、氫氧燃料電池在酸性介質中的正極反應:O2+4e-+2H2O=4OH- |
| D、汽車用的鉛蓄電池充電時陽極反應:PbSO4+2H2O-2e-═PbO2+4H++SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:
 已知水在25℃和95℃時,其電離平衡曲線如圖所示:
已知水在25℃和95℃時,其電離平衡曲線如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:
| 選項 | 現象 | 原因或結論 |
| A | 在 H2O2中加入MnO2,能加速H2O2的分解速率 | MnO2降低了反應所需的活化能 |
| B | 向5mL 0.005mol?L-1FeCl3溶液中加入5mL 0.015mol?L-1KSCN溶液,溶液呈紅色,再滴加幾滴1mol?L-1KSCN溶液,溶液顏色加深 | 增大反應物濃度,平衡向正反應方向移動 |
| C | 將盛有NO2氣體的密閉容器浸泡在熱水中,容器內氣體顏色變深 | 該反應△H<0,平衡向生成NO2方向移動 |
| D | 在密閉容器中有反應:A+xB(g)?2C(g).達到平衡時測得c(A)為0.5mol/L,將容器容積擴大到原來的兩倍,測得c(A)為0.4mol/L-1 | A非氣體、x=1 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、標準狀況下,22.4L酒精含有的分子數約為1NA |
| B、常溫常壓下,1.06g Na2CO3含有的Na+離子數為0.02NA |
| C、通常狀況下,1NA個CO2分子占有的體積為22.4L |
| D、1NA氧原子的質量(以g為單位)在數值上約等于其相對原子質量 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、NaOH、Ca(OH)2、NH3?H2O |
| B、NH4Cl、CH3COOH、Na2S |
| C、HBr、HCl、BaSO4 |
| D、HClO、NaF、Ba(OH)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 物質 | X | Y | Z |
| 初始濃度/mol?L-1 | 0.1 | 0.2 | 0 |
| 平衡濃度/mol?L-1 | 0.05 | 0.05 | 0.1 |
| A、500 |
| B、600 |
| C、1 200 |
| D、1 600 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com