
【題目】(16分)某學生欲用已知物質的量濃度的鹽酸來測定未知物質的量濃度的氫氧化鈉溶液時,選擇甲基橙作指示劑。請填寫下列空白:
(1)用標準的鹽酸溶液滴定待測的氫氧化鈉溶液時,左手把握酸式滴定管的活塞,右手搖動錐形瓶,眼睛注視_______ ________。直到因加入一滴鹽酸后,溶液由黃色變為橙色,并_______________為止。
(2)下列操作中可能使所測氫氧化鈉溶液的濃度數值偏低的是_______________
(A)酸式滴定管未用標準鹽酸溶液潤洗就直接注入標準鹽酸溶液
(B)滴定前盛放氫氧化鈉溶液的錐形瓶用蒸餾水洗凈后沒有干燥
(C)酸式滴定管在滴定前有氣泡,滴定后氣泡消失
(D)讀取鹽酸體積時,開始仰視讀數,滴定結束時俯視讀數
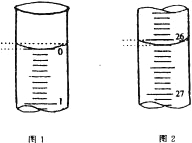
(3)若滴定開始和結束時,酸式滴定管中的液面如圖所示:則起始讀數為_________mL,終點讀數為_____________mL;所用鹽酸溶液的體積為______________ mL。
(4)某學生根據三次實驗分別記錄有關數據如下表:
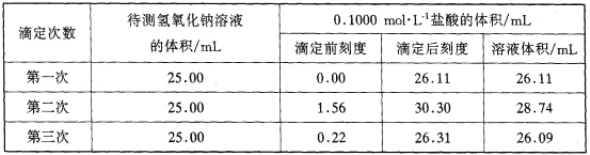
請用上述數據列式計算該氫氧化鈉溶液的物質的量濃度 。
科目:高中化學 來源: 題型:
【題目】含氧有機物甲可用來制取多種有用的化工產品,合成路線如圖:
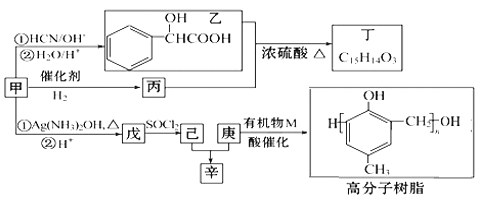
已知:Ⅰ.RCHO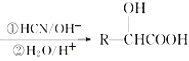
Ⅱ.RCOOH![]() RCOCl
RCOCl![]() RCOOR’(R、R’代表烴基)
RCOOR’(R、R’代表烴基)
(1)甲的含氧官能團的名稱是___。寫出檢驗該官能團常用的一種化學試劑的名稱___。
(2)寫出己和丁的結構簡式:己__,丁__。
(3)乙有多種同分異構體,屬于甲酸酯,含酚羥基,且酚羥基與酯的結構在苯環鄰位的同分異構體共有___種。
(4)在NaOH溶液中發生水解反應時,丁與辛消耗NaOH的物質的量之比為__。
(5)庚與M合成高分子樹脂的化學方程式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲醇被稱為21世紀的新型燃料,工業上在一定條件下可利用反應I和II來制備:
(1)已知在25°C、101kPa下,1 g甲醇燃燒生成CO2和液態水時放熱22.68 kJ,則表示燃燒熱的熱化學方程式為_______________________。
(2)將1.0 molCH4和2.0 molH2O(g)通入容積為10 L密閉容器中,CH4(g)+H2O(g)![]() CO(g)+3H2(g)(I),CH4的轉化率與溫度、壓強的關系如圖所示:
CO(g)+3H2(g)(I),CH4的轉化率與溫度、壓強的關系如圖所示:
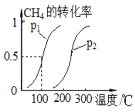
①該反應的△H______0,圖中的p1 ____ p2(填“<”、“>”或“=”)
②已知100℃時達到平衡所需的時間為5 min,則用H2表示的平均反應速率為________________,該反應的平衡常數為_______(mol·L-1)2
(3)在壓強為0.1MPa條件下,amolCO與3amolH2的混合氣體在催化劑作用下能自發反應生成甲醇:CO(g)+2H2(g)![]() CH3OH(g) △H<0(Ⅱ)若容器的容積不變,下列措施可增大甲醇產率的是___________(填序號).
CH3OH(g) △H<0(Ⅱ)若容器的容積不變,下列措施可增大甲醇產率的是___________(填序號).
A.升高溫度 B.將CH3OH(g)從體系中分離出來
C.恒容下充入He,使體系的總壓強增大 D.再充入amolCO和3amolH2.
(4)為提高燃燒效率,某燃料電池以甲醇原料,NaOH溶液為電解質,其負極電極反應式為______________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】炭黑是霧霾中的重要顆粒物,研究發現它可以活化氧分子,生成活化氧。活化過程的能量變化模擬計算結果如圖所示。活化氧可以快速氧化SO2。下列說法正確的是

A. 每活化一個氧分子吸收0.29eV能量
B. 水可使氧分子活化反應的活化能降低0.42eV
C. 氧分子的活化是O-O的斷裂與C-O鍵的生成過程
D. 炭黑顆粒是大氣中SO2轉化為SO3的催化劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:含C=C的物質(烯烴)一定條件下能與水發生加成反應,生成醇(含羥基的烴的衍生物);有機物A-D間存在圖示的轉化關系。下列說法不正確的是
![]()
A.D結構簡式為CH3COOCH2CH3B.A能使酸性高錳酸鉀溶液褪色
C.B與乙酸發生了取代反應D.可用B萃取碘水中的碘單質
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的電解液,電解Na2PbCl4溶液生成Pb的裝置如圖所示。
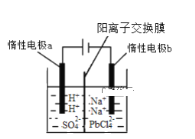
①寫出電解時陰極的電極反應式_____________。
②電解過程中通過陽離子交換膜的離子主要為________。
③電解過程中,Na2PbCl4電解液濃度不斷減小,為了恢復其濃度,應該向___________極室(填“陰”或者“陽”)加入____________(填化學式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于反應2SiHCl3(g)= SiH2Cl2(g)+SiCl4(g) ΔH1=+48 kJ·mol-1,采用大孔弱堿性陰離子交換樹脂催化劑,在323 K和343 K時SiHCl3的轉化率隨時間變化的結果如圖所示。
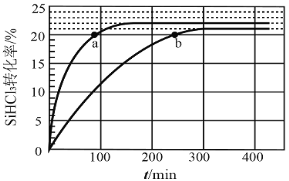
①343 K時反應的平衡轉化率α=_________%。平衡常數K343 K=__________(保留2位小數)。
②在343 K下:要提高SiHCl3轉化率,可采取的措施是__________,要縮短反應達到平衡的時間,可采取的措施有_____________。
③比較a、b處反應速率大小:υa______υb(填“大于”“小于”或“等于”)。反應速率υ=υ正υ逆=![]() ,k正、k逆分別為正、逆向反應速率常數,x為物質的量分數,計算a處
,k正、k逆分別為正、逆向反應速率常數,x為物質的量分數,計算a處![]() =________(保留1位小數)。
=________(保留1位小數)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種藥物中間體(G)的一種合成路線如圖:

已知:
請回答下列問題:
(1)R的名稱是__;R中官能團名稱是__。
(2)M→N的反應類型是__。P的結構簡式為__。
(3)H分子式是__。
(4)寫出Q→H的化學方程式:__。
(5)T是一種與R具有相同官能團的芳香化合物(且組成元素種類相同),T的相對分子質量比R多14。T有__種結構。其中,在核磁共振氫譜上有5組峰且峰的面積比為1:1:2:2:2的結構簡式可能有__。
(6)以1,5-戊二醇(![]() )和硝基苯為原料(其他無機試劑自選)合成
)和硝基苯為原料(其他無機試劑自選)合成![]() ,設計合成路線:__。
,設計合成路線:__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】取A、B兩份物質的量濃度相等的NaOH溶液,體積均為50 mL,分別向其中通入一定量的CO2后,再分別稀釋到100 mL,在稀釋后的溶液中分別逐滴加0.1 mol/L的鹽酸,產生的CO2的體積(標準狀況)與所加鹽酸的體積關系如圖所示:

(1)原NaOH溶液的物質的量濃度_________________。
(2)B份混合溶液與鹽酸反應產生氣體的最大體積為________mL(標準狀況)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com