
分析 (1)反應中化合價降低的元素被還原;
(2)冶煉過程產生大量SO2,處理方案中合理的分析是二氧化硫是污染性氣體,不能排放到空氣中,可以吸收利用;
(3)三價鐵具有氧化性,能將碘離子氧化;
(4)a、氧化鋁是兩性氧化物,能和強酸以及強堿反應;
b、亞鐵離子能被高錳酸鉀溶液氧化,使的高錳酸鉀溶液褪色.
解答 解:(1)化合價降低的元素Cu、O,在反應中被還原,故答案為:Cu、O;
(2)冶煉過程產生大量SO2.分析下列處理方案:
a.二氧化硫是污染性氣體,高空排放會污染空氣,處理不合理,故a錯誤;
b.可以利用吸收二氧化硫生成硫酸,用于制備硫酸,故b合理;
c.用純堿溶液吸收二氧化硫可以制Na2SO4,故c合理;
d.用濃硫酸不能吸收二氧化硫,故d不合理;
故答案為:b、c;
(3)三價鐵具有氧化性,能將碘離子氧化,S2O82-能將亞鐵離子氧化,原理為:2Fe3++2I-=2Fe2++I2,S2O82-+2Fe2+=2SO42-+2Fe3+,
故答案為:2Fe3++2I-=2Fe2++I2;S2O82-+2Fe2+=2SO42-+2Fe3+;
(4)a.氧化鋁是兩性氧化物,能和強酸以及強堿反應,6H++AI2O3=3H2O+2Al3+,除去鋁離子的反應是利用過量氫氧化鈉溶液和鋁離子反應生成四羥基合鋁,
故答案為:Al3++4OH-=2H2O+AlO2-;
b.高錳酸鉀溶液能氧化亞鐵離子,使得高錳酸鉀溶液褪色,故答案為:稀硫酸、KMnO4溶液;稀硫酸浸取爐渣所得溶液使KMnO4溶液褪色.
點評 本題是對金屬的化學性質的考查,要求學生熟記教材知識,學以致用,綜合性較強,難度中等.


科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | b>a>c | B. | c>a>b | C. | a>b>c | D. | a=b=c |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 近年來“霧霾”污染日益嚴重,原因之一是機動車尾氣中含有NO、NO2、CO等氣體.為減少“霧霾”的發生,可采取以下措施:
近年來“霧霾”污染日益嚴重,原因之一是機動車尾氣中含有NO、NO2、CO等氣體.為減少“霧霾”的發生,可采取以下措施:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | A | B | C | D |
| 實驗裝置圖 |  | 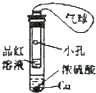 |  | 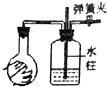 |
| 實驗現象 | U形管右側液面下降 | 小試管中品紅溶液褪色 | 加入少量酚酞,溶液變淺紅色 | 關閉彈簧夾,雙手捂住圓底燒瓶,導管中水柱上升后靜止不動 |
| 實驗結論 | 該條件下鐵釘發生吸氧腐蝕 | 證明二氧化硫具有還原性 | 證明Na2CO3能夠發生水解 | 該裝置氣密性良好 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗操作 | 實驗現象 | 實驗結論 |
| A | NaHCO3溶液與NaAlO2溶液混合 | 生成白色沉淀 | 結合H+的能力: CO32-<AlO2- |
| B | 常溫下,相同的鋁片分別投入足量的稀、濃硫酸中 | 濃硫酸中鋁片先溶解完 | 反應物濃度越大,反應速率越快 |
| C | 向2mL 2%的CuSO4溶液中加入0.5mL 1%的NaOH溶液,振蕩后加入幾滴有機試劑X的溶液,加熱 | 未出現磚紅色沉淀 | 有機試劑X中不含醛基 |
| D | 2mL 0.1mol/L的NaOH溶液中滴加2滴0.1mol/L的MgCl2溶液,再滴加2滴0.1mol/L的FeCl3溶液 | 白色沉淀轉化為紅褐色沉淀 | 溶解度: Mg(OH)2>Fe(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Al3+ Na+ AlO2- Cl- | B. | K+ Na+ Cl- CO32- | ||
| C. | Fe3+ Na+ Cl- HCO3- | D. | SO42- Fe2+ H+ NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
 氨催化氧化是硝酸工業的基礎,在某催化劑作用下只發生主反應①和副反應②,有關物質產率與溫度的關系如圖
氨催化氧化是硝酸工業的基礎,在某催化劑作用下只發生主反應①和副反應②,有關物質產率與溫度的關系如圖| A. | 在400℃時,反應①未達平衡,反應②達到平衡 | |
| B. | 800℃后再升高溫度,反應①的平衡逆向移動;反應②的平衡正向移動 | |
| C. | 加壓可提高NH3生成NO的轉化率 | |
| D. | N2氧化為NO的熱化學方程式為:N2(g)+O2(g)?2NO(g)△H=-181.5 kJ•mol-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com